
Forscher der Universität des Saarlandes und des Imperial College in London könnten einen wichtigen Baustein für den technologischen Fortschritt entdeckt haben.
Chemiker um David Scheschkewitz, Professor für Allgemeine und Anorganische Chemie, haben ein Silicium-Molekül entwickelt, das extrem stabil ist und aufgrund seiner elektronischen Eigenschaften zukünftig zum Beispiel in der Halbleiterindustrie eine wichtige Rolle spielen könnte.
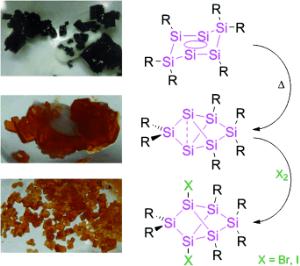
Die Wissenschaftler veröffentlichten die Entdeckung des sogenannten Si-verbrückten Persilapropellans in der renommierten Fachzeitschrift Angewandte Chemie [siehe unten].
Das natürliche Vorbild für das Silicium-Molekül ist Benzol, eine Verbindung aus sechs Kohlenstoff- und sechs Wasserstoffatomen. Benzol ist die energetisch stabilste Verbindung aus diesen Atomen und von überragender Bedeutung für viele Bauelemente in allen Bereichen der Chemie. Im Gegensatz zum Benzol, das flach und ringförmig angelegt ist, besitzt das verbrückte Persilapropellan aber eine dreidimensionale, käfigartige Struktur. Chemiker weltweit haben bisher immer versucht, die flache Benzolstruktur aus Wasserstoff und Sauerstoff zu imitieren, indem sie Silicium an die Stelle des Kohlenstoffs setzen. "Solche Moleküle sind aber im Fall des Siliciums instabil, wodurch mögliche Anwendungen erschwert werden", erklärt David Scheschkewitz.
"Unser Si-verbrücktes Persilapropellan hingegen könnte als Baustein für zukünftige Anwendungen in der Materialchemie interessant sein", so Scheschkewitz weiter. Potenziell interessant seien solche Polymere beispielsweise für die OLED-Technologie, also organische Leuchtdioden, die im Gegensatz zu bisher gebräuchlichen LEDs deutlich dünner gebaut werden und zum Beispiel für papierdünne Monitore ("elektronisches Papier") verwendet werden können.
Auch für den Einsatz in der Solarzellentechnologie und in der Computerindustrie könnte das Molekül nutzbar sein. "Gängige Halbleitertechnik basiert im Wesentlichen auf Silicium", erklärt David Scheschkewitz, der vor Kurzem vom Imperial College in London an die Uni des Saarlandes kam. "Es wird immer Mikroelektronik auf Siliciumbasis geben, selbst wenn es beispielsweise irgendwann marktfähige Quantencomputer geben sollte", sagt Scheschkewitz. Und zwischen solchen Geräten muss die Kommunikation stimmen. Das verbrückte Persilapropellan könnte dank seines ungesättigten Charakters, also freier Bindungen, die es eingehen kann, und extremen energetischen Stabilität auf molekularer Ebene als Schnittstelle zwischen solchen Geräten dienen.
Die Entdeckung ist ein zufälliges Resultat aus einem vorangegangenen Projekt von David Scheschkewitz. Kai Abersfelder, Doktorand am Lehrstuhl von Professor Scheschkewitz, testete eine chemische Reaktion mit einer völlig anderen Zielstellung. "Von besagtem Experiment habe ich ihm eigentlich abgeraten", erinnert sich David Scheschkewitz amüsiert. "Aber das ist wieder einmal ein schöner Beweis dafür, wie oft in der Forschung der Zufall eine Rolle spielt."
Zusatzinformationen:
Kai Abersfelder, Dr. Andrew J. P. White, Dr. Raphael J. F. Berger, Prof. Dr. Henry S. Rzepa, Prof. Dr. David Scheschkewitz:
Ein stabiles Derivat des globalen Minimums der Si6H6-Potentialhyperfläche.
In: Angewandte Chemie; online veröffentlicht am 04. Juli 2011, DOI 10.1002/ange.201102623
Quelle: Universität des Saarlandes, Saarbrücken
Aktualisiert am 06.07.2011.
Permalink: https://www.internetchemie.info/news/2011/jul11/si-persilapropellan.php
© 1996 - 2024 Internetchemie ChemLin