Thioharnstoffdioxid ist der Trivialname für die organische Verbindung mit der systematischen chemischen Bezeichnung Aminoiminomethansulfinsäure, die den Stoffgruppen der Amidine und der Sulfinsäuren zugeordnet wird.
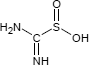
In reinem Zustand zeigt sich Thioharnstoffdioxid als weiße bis hellgelbes, geruchlose Substanz, die bei 126 °C schmilzt, nur wenig in Wasser löslich ist und eine starkes Reduktionsmittel darstellt.
Die Verbindung zersetzt sich exotherm oberhalb 126 ° C unter Emission von schädlichen Gasen (Schwefeloxide, Ammoniak, Kohlenmonoxid, Stickstoffoxiden und Schwefelwasserstoff) sowie Kohlendioxid. Längere Erwärmung auf Temperaturen über 50 ° C oder der Einfluss von Feuchtigkeit kann zu sichtbarer Zersetzung der Substanz führen. Thioharnstoffdioxid reizt die Haut und die Schleimhäute und wirkt ätzend auf das Augengewebe.
Synthese von Thioharnstoffdioxid
Die Herstellung der Aminoiminomethansulfinsäure gelingt durch einfache Umsetzung von Thioharnstoff mit Wasserstoffperoxid, wodurch die Schwefel-Gruppe oxidiert wird. Optimale Reaktionsbedingungen sind Temperaturen unter 10 °C sowie ein pH-Wert zwischen 3 und 5, um die Bildung von Disulfid-Varianten als Nebenprodukte zu vermeiden.
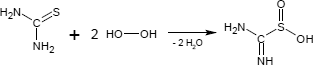
Eine weitere Synthese-Möglichkeit ist die Reaktion von Thioharnstoff mit einem Überschuss an Chlordioxid, wobei jedoch Chlor freigesetzt wird.
Verwendung
Die Papier- und Textil-Industrie nutzt Thioharnstoffdioxid zur reduktiven Bleiche von Textilien, Wolle, Seide etc. und als Reduktionsmittel für Küpenfarbstoffe.
Datenblatt: Thioharnstoffdioxid
Gefahrenhinweise und Sicherheit:




Gefahr
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit)
Diese Substanz ist selbstentzündlich und kann Feuer fangen, ist gesundheitsschädlich beim Verschlucken, verursacht schwere Augenschäden, kann die Organe durch länger andauernde oder wiederholte Exposition schädigen, ist gesundheitsschädlich beim Einatmen, verursacht Hautreizungen und kann zu Reizungen der Atemwege führen.
Quellen und weitere Informationen:
[1] - Michael Hoffmann, John O. Edwards:
Kinetics and mechanism of the oxidation of thiourea and N,N´-dialkylthioureas by hydrogen peroxide.
In: Inorganic Chemistry, (1977), DOI 10.1021/ic50178a069.
[2] - Gyula Rabai, Robert T. Wang, Kenneth Kustin:
Kinetics and mechanism of the oxidation of thiourea by chlorine dioxide.
In: International Journal of Chemical Kinetics, (1993), DOI 10.1002/kin.550250106.
Aktualisiert am 10.12.2018.
Permalink: https://www.internetchemie.info/chemie-lexikon/stoffe/t/thioharnstoffdioxid.php
© 1996 - 2026 Internetchemie ChemLin