Amine - eine Gruppe stickstoffhaltiger organischer Verbindungen - spielen in vielen Bereichen der Natur, im täglichen Leben und in der chemischen Industrie eine wichtige Rolle.
So sind Biogene Amine - durch Decarboxylierung von Aminosäuren im Körper entstandene Substanzen - wichtige Schlüsselverbindungen als Vorstufen von Hormonen und Vitaminen, als Neurotransmitter, als Pharmaka u. a.Einige flüchtige Amine, ebenfalls Abbauprodukte von Aminosäuren, sind uns als Verursacher des typischen Fischgeruchs bekannt.
Im technischen Bereich finden Amine als Ausgangssubstanzen und Zwischensubstanzen für eine ganze Reihe von Produkten Anwendung: Lösungsmittel, Textilhilfsmittel, Tenside, Bakterizide, Additive, Arzneimittel etc. und in Form aromatischer Amine für die Herstellung von (Azo-)farbstoffen.
Heutige großtechnische Aminsynthesen verlaufen häufig über mehrere Stufen. Es besteht daher ein großer Bedarf an großtechnisch umsetzbaren Aminsynthesen, die möglichst hochselektiv und atomökonomisch sein und den immer stärkeren Anforderungen an eine nachhaltige Chemie gerecht werden sollen.
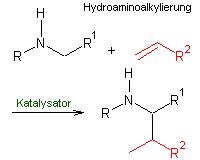
Eine dieser Synthesen ist die Hydroaminoalkylierung zur Herstellung verzweigter Alkylamine durch die Addition einer α-C-H-Bindung an ein Alken (siehe Reaktionsschema).
In den vergangenen Jahren berichteten mehrere Forschungsgruppen über Weiterentwicklungen der Hydroaminoalkylierung von Alkenen unter Einsatz verschiedener Katalysatoren. In einem aktuellen Artikel der Angewandten Chemie fanden unter anderem die Forschungsergebnisse der Arbeitsgruppe um Prof. Dr. Sven Doye vom Institut für Reine und Angewandte Chemie an der Universität Oldenburg besondere Beachtung [1].
Professor Doye sowie seine Mitarbeiter Dipl.-Chem. Raphael Kubiak und Dipl.-Chem. Insa Prochnow beschreiben titankalysierte Hydroaminoalkylierungen und stufen diese als potentiell äußerst interessante, einstufige, abfallfreie und somit ressourcenschonende Möglichkeit zur Herstellung komplexer Amine aus einfacheren Ausgangsverbindungen ein [2].
Doye und Mitarbeiter beschreiben im wesentlichen 3 Reaktionen: Die selektive Bildung von Cyclohexylaminen, intermolekulare Hydroaminoalkylierungen einiger N-arylierter Amine sowie die Reaktionen von 1-Octen mit N-Methylanilin in Anwesenheit verschiedener Ti-Katalysatoren.
Im Ergebnis weisen die Arbeiten neue Wege zur Herstellung von primären und sekundären Aminen. Bisher noch hohe Reaktionstemperaturen und Reaktionszeiten erfordern jedoch Optimierungen der Katalysatoren, was sicherlich auch zu einer Erweiterung der Anwendungsmöglichkeiten und der Selektivität der katalytischen Hydroaminoalkylierung führen wird.
Zusatzinformationen:
Prof. Dr. Peter W. Roesky:
Katalytische Hydroaminoalkylierung.
In: Angewandte Chemie; online veröffentlicht am 13. Mai 2009, DOI 10.1002/ange.200900735
Raphael Kubiak, Insa Prochnow, Prof. Dr. Sven Doye:
Titankatalysierte Hydroaminoalkylierung von Alkenen durch C-H-Aktivierung an sp3-Zentren in der alpha-Position zum Stickstoffatom.
In: Angewandte Chemie; online veröffentlicht am 29. Dezember 2008, DOI 10.1002/ange.200805169
Quelle: Carl von Ossietzky-Universität, Oldenburg
Aktualisiert am 11.07.2009.
Permalink: https://www.internetchemie.info/news/2009/jul09/katalytische-hydroaminoalkylierung.php
© 1996 - 2026 Internetchemie ChemLin