|
|
|
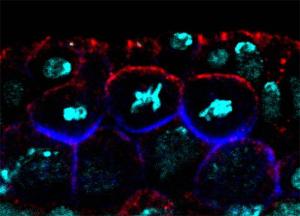
Ein Embryo der Fruchtfliege Drosophila wurde angefärbt für die Proteine Bazooka (rot) und Miranda (blau). Die DNA ist in türkis dargestellt. Die drei großen runden Zellen in der Mitte sind neurale Stammzellen, die sich gerade in der Teilung befinden. Die Aufnahme wurde mit einem konfokalen Laser Scanning Mikroskop gemacht.
[Bildquelle: CMPB/AG Prof. Wodarz]
|
Mit ihren Untersuchungen setzten sie bei einem bekannten Phänomen an: Die asymmetrische Zellteilung befähigt eine Stammzelle zur Bildung von zwei Tochterzellen mit unterschiedlichen Zell-Schicksalen. Eine Tochterzelle kann sich z.B. zu einer Knochen-, Blut- oder Nervenzelle entwickeln, wohingegen die zweite ihre eigene Identität als Stammzelle behält und sich weiterhin teilen kann. Eine wesentliche Voraussetzung für solch eine asymmetrische Zellteilung ist die "Polarisierung" der Stammzelle. Dafür müssen sich bestimmte Proteine schon vor der Teilung in der einen oder der anderen Hälfte der sich teilenden Zelle gruppieren. Die Göttinger Wissenschaftler können nun zeigen, welche molekularen Mechanismen die Anreicherung des für die Polarisierung der Stammzelle essentiellen Proteins Bazooka an einem bestimmten Pol der Zelle steuern. "Wir konnten außerdem beobachten, dass eine Störung dieser Abläufe direkte Auswirkungen auf die Polarität der Stammzelle hat", sagt Prof. Dr. Andreas Wodarz, Leiter der Studie und Direktor der Abteilung Stammzellbiologie an der Universitätsmedizin Göttingen. Störungen der Zellpolarität und asymmetrischen Zellteilung können zu schwerwiegenden Erkrankungen führen und werden z.B. mit der Entstehung von Krebs in Zusammenhang gebracht. Kontrolle der Zellpolarität Einige der Proteine, die beim Prozess der Polarisierung in den neuronalen Stammzellen der Fruchtfliege eine Rolle spielen, sind bereits bekannt: Das Bazooka Protein ist eines der wichtigsten. Es konzentriert sich vor der Teilung in einem Komplex mit zwei weiteren Proteinen namens PAR-6 und aPKC nur auf der einen, der nach oben gerichteten (apikalen) Seite der Zelle. Proteine wie Numb oder Miranda hingegen gruppieren sich auf der gegenüberliegenden, nach unten gerichteten (basalen) Zellseite. Das Protein Bazooka gelangt infolgedessen nur in eine der entstehenden Tochterzellen, und zwar in diejenige, die ihre Identität als Stammzelle behält. Prof. Wodarz und sein Team haben nun untersucht, welche Faktoren zu dieser asymmetrischen Verteilung von Bazooka beitragen. "Es ist bekannt, dass Bazooka von einem anderen Protein namens PAR-1 an zwei Stellen phosphoryliert wird. Doch ob dieser Vorgang für die eindeutige Ausrichtung des Proteins Bazooka bedeutsam ist, war ungeklärt", sagt der am Forschungsprojekt maßgeblich beteiligte Nachwuchswissenschaftler Dr. Michael Krahn. "Wir haben nun gefunden, dass Protein Phosphatase 2A (PP2A) direkt an Bazooka bindet und die von PAR-1 an-gehängten Phosphate an einer Stelle entfernt. PP2A ist also ein direkter Antagonist von PAR-1", sagt der Wissenschaftler. Eine Blockade von PP2A - und somit eine konstant erhöhte Phosphorylierung von Bazooka - führte überraschenderweise zu einer basalen statt apikalen Anordnung des Bazooka Proteins und folglich zu einer kompletten Umkehrung der Zellpolarität. "Generell deutet dies daraufhin, dass ein Gleichgewicht von PAR-1 und PP2A Effekten für die korrekte Positionierung von Bazooka und eine richtige Polarisierung der Zelle essentiell ist", so Prof. Wodarz. Zum DFG Forschungszentrum Molekularphysiologie des Gehirns: Das seit 2002 an der Universitätsmedizin Göttingen angesiedelte DFG Forschungszentrum Molekularphysiologie des Gehirns (CMPB) hat sich das Ziel gesetzt, molekulare Prozesse und Interaktionen in Nervenzellen detailliert zu analysieren. Die Forschungen sollen helfen, langfristig Therapien für psychiatrische, neurologische und neurodegenerative Erkrankungen zu verbessern und weiterzuentwickeln.
|