Wasser ist ein Hauptbestandteil von Kometen, die deswegen auch als "schmutzige Schneebälle" bezeichnet werden.
Einer internationalen Forschergruppe um Andreas Wolf vom Max-Planck-Institut für Kernphysik in Heidelberg gelang es jetzt, die Entstehung von Wassermolekülen im Weltraum detailliert zu entschlüsseln.
Überraschend stellten sie dabei fest, dass die H2O-Moleküle in den ultrakalten Kometen als 60000 Grad heiße Teilchen entstehen.
Für ihre Forschung verwendeten die Physiker indes kein Teleskop, sondern einen Teilchenbeschleuniger [Physical Review Letters, siehe unten].
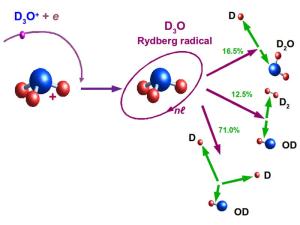
In Kometen und interstellaren Wolken ist der Ausgangsstoff des Wassers das positiv geladene Hydronium-Ion H3O+. Dieses Molekülion lässt sich von der Erde aus mit Teleskopen nachweisen. In den kosmischen Wolken fliegen normalerweise auch negativ geladene Elektronen umher, so dass es häufig zu Zusammenstößen kommt. Dabei wird das Hydronium-Ion zu dem neutralen aber instabilen Molekül H3O, das sofort zerfällt. "Hierfür stellt die Natur drei Möglichkeiten zur Wahl", erklärt Andreas Wolf: Entweder entsteht H2O plus H, OH plus H2 oder OH plus zwei H-Atome. Ein Ziel der aktuellen Forschung ist es herauszufinden, mit welcher Häufigkeit die drei Zerfallsarten auftreten und Wasser entsteht.
Wolf und Kollegen gingen dieser Frage nach, indem sie die Elektronenanlagerung im Labor nachstellten. Hierfür verwendeten sie den Heidelberger Testspeicherring, eine Art Rennbahn mit 55 Meter Umfang, auf der geladene Teilchen von Magneten geführt herumrasen.
In diesen Ring speisen die Forscher Hydronium-Ionen ein, genauer D3O+, also Hydronium-Ionen aus schweren Wasserstoffatomen, die sich für die Experimente besser eignen als gewöhnlicher Wasserstoff. An einer Stelle im Ring strömen zudem von außen Elektronen hinein, die die Ionen auf einem knapp zwei Meter langen Teilstück begleiten und dann den Ring wieder verlassen. Das geschieht bei jedem Umlauf, also mehrere hunderttausend Mal pro Sekunde.
In dem Elektronenbad lagern sich nun - fast so wie im Weltraum - Elektronen mit Hydronium-Ionen zu Molekülen zusammen, die sofort zerfallen. Die Bruchstücke sind aber elektrisch neutral. Sie reagieren deswegen nicht auf das Magnetfeld und fliegen aus dem Speicherring heraus. An dieser Stelle hat Wolfs Gruppe einen Detektor installiert, der die auftreffenden Teilchen registriert. Dieses empfindliche Gerät entstand in Zusammenarbeit mit Kollegen des israelischen Weizmann-Instituts in Rehovot.
Mit bis zu tausend "Bildern" pro Sekunde registriert der Detektor Molekülmassen und Impulse aller Zerfallsprodukte. Aus diesen Daten lassen sich die Vorgänge beim Anlagern der Elektronen und anschließenden Auseinanderbrechen des Moleküls exakt rekonstruieren.
Das erste wichtige Ergebnis: Bei der Elektronen-Anlagerung zerfällt das Hydronium zu 16,5 Prozent zu Wasser. "Das ist ein recht hoher Wert", sagt Wolf. "Wahrscheinlich ist die Elektronenanlagerung an Hydronium-Ionen der wichtigste Wasserproduktionsweg in interstellaren Wolken und Kometen."
Am häufigsten, nämlich zu 71 Prozent, zersplittert das Hydronium-Ion jedoch in die drei Bestandteile OH plus zwei H-Atome. Warum das so ist, können die Forscher jetzt erklären. Wenn sich das Elektron an das Ion anlagert, wird dabei Bindungsenergie frei. Diese nimmt das gesamte Molekül auf und fängt an zu schwingen, ähnlich wie eine Spiralfeder, die man spannt und loslässt. "Wir haben zur Überraschung aller herausgefunden, dass die Moleküle mit der maximal möglichen Energie schwingen", sagt Wolf. Damit ist jedes Molekül bei der Elektronenanlagerung kurz vor dem Zerreißen und zerbricht eben eher in drei als in zwei Teile.
Die hohe Schwingungsenergie lässt sich auch in eine Temperatur umrechnen. Dabei kommen die Physiker auf 60 000 Grad Celsius: Wasser kommt also heiß in die Welt.
Die neuen Erkenntnisse haben noch weitere Auswirkungen. Zum einen gehen sie als Parameter in Computermodelle ein, mit denen das komplexe Reaktionsnetz in interstellaren Wolken berechnet wird. Zum anderen erklären sie Beobachtungen einiger Kometen. In deren Infrarotspektren hatten Astronomen Banden "heißer" Wassermoleküle gefunden, was sich jetzt erklären lässt: Die neu gebildeten Wassermoleküle geben ihre Schwingungenergie schrittweise ab, und bei jeder weiteren "Abregungsstufe" senden sie Infrarotstrahlung aus. Und nicht zuletzt geben die neuen Messergebnisse ungeahnt detaillierte Aufschlüsse über die elektronischen Vorgänge in einem Hydronium-Ion und dienen so als Input für quantenmechanische Modelle dieser Moleküle.
Zusatzinformationen:
H. Buhr, J. Stützel, M. B. Mendes, O. Novotný, D. Schwalm, M. H. Berg, D. Bing, M. Grieser, O. Heber, C. Krantz, S. Menk, S. Novotny, D. A. Orlov, A. Petrignani, M. L. Rappaport, R. Repnow, D. Zajfman, A. Wolf:
Hot Water Molecules from Dissociative Recombination of D3O+ with Cold Electrons.
In: Physical Review Letters; 105, 103202; online veröffentlicht am 03. September 2010, DOI 10.1103/PhysRevLett.105.103202
Quelle: Max-Planck-Institut für Kernphysik, Heidelberg
Aktualisiert am 11.09.2010.
Permalink: https://www.internetchemie.info/news/2010/sep10/interstellare-wasserproduktion.php
© 1996 - 2026 Internetchemie ChemLin