Stickstoffmonoxid ist ein farb- und geruchloses Gas. Im Körper des Menschen wirkt es zum Beispiel an so grundlegenden Vorgängen wie der Regulierung des Blutdrucks und der Weiterleitung von Nervenimpulsen im Gehirn mit.
Die Rolle von Stickstoffmonoxid in Pflanzen wird seit Anfang der 1980er-Jahre erforscht.
Dabei zeigt sich immer mehr, dass dieses Gas in die Riege der klassischen Pflanzenhormone einzureihen ist.
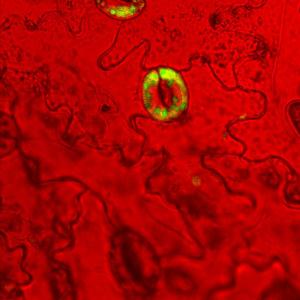
In den Zellen selbst fungiert es als Botenstoff, der für die Bildung und Entwicklung der Wasserleitungsgefäße, für die Regulierung der Öffnungsweite von Spaltöffnungen und für andere Prozesse wichtig ist.
Wenn Forscher den Funktionen des Stickstoffmonoxids nachspüren, machen sie das Gas in der Regel mit speziellen Fluoreszenz-Farbstoffen sichtbar, mit so genannten Diaminofluoreszeinen (DAF). Mit diesen Farbstoffen ist auch eine mikroskopische Analyse von Pflanzengeweben möglich. Bislang vertraute man darauf, dass die Farbstoffe ausschließlich Stickstoffmonoxid nachweisen. Doch das ist nicht immer der Fall, wie die Arbeitsgruppe um den emeritierten Pflanzenphysiologen Professor Werner Kaiser von der Universität Würzburg nachgewiesen hat.
Bildung von Stickstoffmonoxid provoziert
Die Würzburger Botaniker haben im Labor eine Situation nachgeahmt, bei der nach gängiger Lehrmeinung unter anderem Stickstoffmonoxid entsteht: Eine Pflanze wird von einem Schadpilz befallen und produziert daraufhin unter anderem das stickstoffhaltige Gas, um den Angreifer zu schädigen. Die Forscher provozierten diese Reaktion, indem sie einer Suspension von Tabakzellen das Pilz-Protein Cryptogein hinzufügten, das die Verteidigungsreaktion auslöst.
Farbstoffe reagieren mit Wasserstoffperoxid
Aus früheren Untersuchungen wussten die Wissenschaftler: Die Fluoreszenz-Farbstoffe sprechen bei diesem Experiment an, doch eine andere, für Stickstoffmonoxid ebenfalls spezifische Nachweismethode eben nicht. Jetzt fanden sie heraus, warum das so ist: Die Farbstoffe reagieren in diesem Fall gar nicht mit Stickstoffmonoxid, sondern mit ebenfalls entstehendem Wasserstoffperoxid und Peroxidase-Enzymen zu fluoreszierenden Produkten - und sorgen damit für eine falsche Interpretation der Fluoreszenzdaten. Das berichten die Würzburger in der Fachzeitschrift 'Nitric Oxide - Biology and Chemistry' [siehe unten].
"Möglicherweise müssen nun viele frühere Veröffentlichungen, die auf Messungen mit DAF-Fluoreszenzfarbstoffen basieren, unter einem neuen Licht gesehen werden", sagt der Biologe Stefan Rümer. Denn eventuell wurde auch bei anderen Experimenten in Biologie und Medizin nicht Stickstoffmonoxid nachgewiesen, sondern Wasserstoffperoxid.
Zusatzinformationen:
Stefan Rümer, Markus Krischke, Agnes Fekete, Martin J. Mueller, Werner M. Kaiser:
DAF-fluorescence without NO: Elicitor treated tobacco cells produce fluorescing DAF-derivatives not related to DAF-2 triazol.
In: Nitric Oxide; Volume 27, Issue 2, Pages 123 - 135, 15. August 2012, DOI 10.1016/j.niox.2012.05.007
Quelle: Julius-Maximilians-Universität, Würzburg
Aktualisiert am 11.09.2012.
Permalink: https://www.internetchemie.info/news/2012/sep12/daf-fluoreceine.php
© 1996 - 2026 Internetchemie ChemLin