Mülheim an der Ruhr - Wie wird aus einem Haufen toter Materie ein komplexer Organismus?
Wie entstehen aus leblosen Stoffen organische Moleküle, die schließlich Bausteine für Tiere und Pflanzen bilden?
Dieser Frage gehen Wissenschaftler seit langer Zeit auf den Grund.
Forschern am Max-Planck-Institut für Kohlenforschung in Mülheim an der Ruhr ist es jetzt gelungen, ein Rätsel zu lüften, das sich hinter einer Synthese von organischem Material verbirgt, das Bausteine für Lebewesen bildet.
Die Rolle des Sonnenlichts
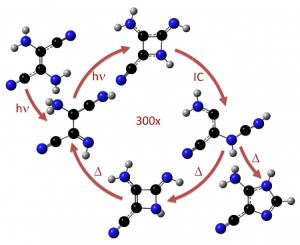
Seit den 1960er Jahren weiß man, dass konzentrierter Cyanwasserstoff (HCN), auch als Blausäure bekannt, sogenannte Imidazole bildet, sobald er mit UV-Licht bestrahlt wird. Imidazole sind ringförmige Schlüsselmoleküle, die bei der Bildung von Nucleinsäuren und deren Bausteinen, den Nucleotiden, eine wichtige Rolle spielen. Wie genau aber die Rolle des Lichts in dieser Reaktion von Blausäure zu Imidazolen ist, konnte bislang nicht geklärt werden. Einer internationalen Forschergruppe um Dr. Mario Barbatti vom Max-Planck-Institut für Kohlenforschung ist es nun gelungen, die Reaktion anhand von Simulationen nachzuvollziehen.
Mit unterschiedlichen Methoden der Computerchemie haben die Wissenschaftler Erstaunliches herausgefunden. Beispielsweise, dass die Reaktion keinesfalls in einer heißen Umgebung stattfinden muss, auch wenn die Sonneneinstrahlung eine große Rolle spielt. "Das hat mit Hitze nichts zu tun, sondern mit Elektronen", erklärt Mario Barbatti.
Hunderte Photonen bis zum entscheidenden Schritt
Die Blausäure durchlaufe während der Reaktion eine ganze Reihe von elektronisch aufgeladenen Stadien. Durch die UV-Strahlen, wie sie von der Sonne ausgestrahlt werden, wird das Molekül in einen "angeregten Zustand" versetzt. Das bedeutet, dass die Elektronen völlig anders verteilt sind als im normalen Zustand. Das verändert die Eigenschaften des Moleküls. "Das passiert in diesem Fall aber sehr schleppend", erklärt Mario Barbatti. Denn die Zerstreuung der Sonnenstrahlen geht zu schnell vonstatten. Jedes Molekül müsse darum mit hunderten von UV-Photonen beschossen werden, bevor endlich der entscheidende Schritt passiert und aus der Blausäure das Imidazol wird.
"Das ist sehr ineffizient und daher wirklich ungewöhnlich", erklärt Mario Barbatti. Darum sei es auch nicht einfach gewesen, die Reaktion rechnerisch nachzuvollziehen, so der Physiker aus Brasilien. Schritt für Schritt haben er und seine Kollegen am Computer mögliche Zwischenstadien errechnet und ausprobiert, viele davon auch wieder verworfen, bevor sie den richtigen Weg gefunden haben, der mit der schnellen Zerstreuung der Energie und den Erkenntnissen aus der Experimentalchemie zusammenpasst.
Reaktionen theoretisch nachvollziehen
Aber warum am Computer - arbeitet man an chemischen Reaktionen nicht normalerweise im Labor? "Einige Zwischenstadien der Reaktion sind zu flüchtig. Sie verschwinden, bevor wir sie sehen können", sagt Barbatti. Die Computerchemie erlaubt es den Forschern jedoch, Reaktionen theoretisch nachzuvollziehen.
"Wie gesagt, kommt es bei dieser Reaktion nicht auf Hitze an", sagt Mario Barbatti. Die Umwandlung von Blausäure zu Imidazolen funktioniere auch in einer kalten Umgebung, beispielsweise in einem Kometen oder im Eis, das auf einem Planeten wie der Erde vorkommt. In solchen Umgebungen ist auch die spontane Bildung von Blausäure viel wahrscheinlicher.
Ihre Ergebnisse hat die Forschergruppe nun in der aktuellen Ausgabe der Fachzeitschrift Angewandte Chemie veröffentlicht.
Zusatzinformationen:
Eliot Boulanger, Dr. Anakuthil Anoop, Dr. Dana Nachtigallova, Prof. Dr. Walter Thiel, Dr. Mario Barbatti:
Photochemical Steps in the Prebiotic Synthesis of Purine Precursors from HCN.
In: Angewandte Chemie; online veröffentlicht am 19. Juni 2013, DOI 10.1002/ange.201303246
Quelle: Max-Planck-Institut für Kohlenforschung, Mülheim an der Ruhr
Aktualisiert am 25.06.2013.
Permalink: https://www.internetchemie.info/news/2013/jun13/purin-vorlaeufer.php
© 1996 - 2026 Internetchemie ChemLin