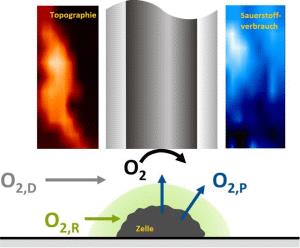
Wie aktiv eine lebende Zelle ist, lässt sich anhand ihres Sauerstoffverbrauchs ablesen.
Die Methode, mit der man diesen Verbrauch bestimmt, haben Bochumer Chemiker nun entscheidend weiter entwickelt.
Problematisch war bislang, dass die Messelektrode den Sauerstoffumsatz in der Umgebung der Zelle wesentlich stärker veränderte als die Zelle selbst. "Das haben wir schon vor 12 Jahren festgestellt", sagt Prof. Dr. Wolfgang Schuhmann vom Lehrstuhl für Analytische Chemie der Ruhr-Universität.
"Nun ist es uns endlich gelungen, die Messelektrode zum Beobachter zu machen."
Gemeinsam mit seinem Team berichtet er in der Zeitschrift 'Angewandte Chemie' [siehe unten].
Messelektroden präzise positionieren
Zellen brauchen Sauerstoff für verschiedene Stoffwechselvorgänge, etwa um Glukose abzubauen. Um den Verbrauch zu messen, müssen Forscher sehr kleine Signale in einem großen Hintergrundrauschen detektieren. Sie nutzen dazu die elektrochemische Rastermikroskopie, für die sie Elektroden mit einem Durchmesser von fünf Mikrometer in einem Abstand von 200 Nanometer von der Zelle platzieren müssen. Dafür hat das RUB-Team im Lauf der letzten Jahre ein spezielles Verfahren entwickelt, mit dem sich der Abstand der Elektrode zur Zelle präzise kontrollieren lässt.
Den Zellen mit Mikroelektroden Konkurrenz machen
Mit der Elektrode erzeugen die Forscher zunächst Sauerstoff in der wässrigen Umgebung der Zelle; dann messen sie, wie viel die Zelle davon verwertet. Zu diesem Zweck legen sie zu Beginn ein bestimmtes Potenzial an der Elektrode an. Dieses bewirkt, dass dem Wasser in der Zellumgebung Elektronen entzogen werden; es entsteht Sauerstoff. Den Sauerstoff kann die Zelle für ihren Stoffwechsel nutzen; gleichzeitig machen die Forscher ihr aber mit der Mikroelektrode Konkurrenz. Sie ändern das Potenzial an der Elektrode so, dass sich die Reaktion umkehrt: Sauerstoff wird nun zu Wasser umgesetzt. Die dabei fließenden Elektronen messen die Wissenschaftler mit der Elektrode und erhalten so ein Maß für den Sauerstoffverbrauch in der lokalen Umgebung. Je mehr Sauerstoff die Zelle für ihren Stoffwechsel verbraucht, desto weniger Sauerstoff bleibt für die stromerzeugende Reaktion an der Elektrode. Je geringer also der gemessene Stromfluss, desto stärker die Aktivität der Zelle. Bei diesem Verfahren spricht man vom Redoxkompetitionsmodus.
Schnelle Messung
Bei den bisher eingesetzten Verfahren war der durch die Elektrode erzeugte Sauerstoffverbrauch wesentlich größer als der Verbrauch der Zelle. "Die Messung selbst hat die Sauerstoffkonzentration lokal also stärker verändert als der Zellstoffwechsel", erklärt Prof. Schuhmann. Entscheidend war es, die Aktivität der Zelle sehr schnell, nachdem der Sauerstoff an der Mikroelektrode erzeugt worden war, zu messen - nämlich nach 20 Millisekunden. Wartet man länger, so entzieht die Elektrode der Zelle Sauerstoff, anstatt den Sauerstoff aus der Umgebung zu verwenden, den die Forscher zuvor künstlich erzeugten. Drei Faktoren waren also maßgeblich für den Erfolg der Bochumer Methode: die sehr genaue Position der Elektroden, der Redoxkompetitionsmodus und die schnelle Messzeit.
Zusatzinformationen:
Dr. Michaela Nebel, Stefanie Grützke, Prof. Dr. Nizam Diab, Prof. Dr. Albert Schulte, Prof. Dr. Wolfgang Schuhmann:
Visualisierung des O2-Verbrauchs einzelner lebender Zellen mithilfe elektrochemischer Rastermikroskopie: der Einfluss der faradayschen Sondenreaktion.
In: Angewandte Chemie; online veröffentlicht am 29. April 2013, DOI 10.1002/anie.201301098
Quelle: Ruhr-Universität Bochum, RUB
Aktualisiert am 07.05.2013.
Permalink: https://www.internetchemie.info/news/2013/may13/elektrochemische-rastermikroskopie.php
© 1996 - 2026 Internetchemie ChemLin