Radiumsulfat ist eine anorganische Verbindung, die chemisch als das Radium-Salz der Schwefelsäure beschrieben wird.
Bezeichnungen und Identifikatoren
Radiumsulfat
O4SRa
RaSO4
322,081 (g/mol)
7446-16-4
MXQFUMUIEZBICJ-UHFFFAOYSA-L
Englische Bezeichnung
Radium sulfate
Radium sulphate
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Radiumsulfat:
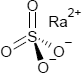
O4SRa oder RaSO4
Mr = 322,0814 g/mol
SMILES: [Ra+2].[O-]S([O-])(=O)=O
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Radiumsulfat. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Reines Radiumsulfat hat unter Standardbedingungen das Aussehen eines weißen bzw. farblosen kristallinen Pulvers, das im Dunkeln leuchtet und nicht in Wasser löslich ist.
- Praktisch unlöslich in Wasser (2,1 mg/L bei 18 °C).
-1474,9 kJ/mol bei 25 °C
Orthorhombische Kristalle, Raumgruppe Pmna, Nr. 62, Gitterkonstanten: a = 912,9(8) pm, b = 553,8(3) pm, c = 731,3(5) pm [vgl. Artem V. Matyskin et al., 2017].
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Radiumsulfat - O4SRa - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Sauerstoff
ΣAr = 63,996 u
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 19,82123 %
17O: 0,00762 %
18O: 0,04073 %
Schwefel
32S: 31,97207 u [94,954 %]
33S: 32,97146 u [0,763 %]
34S: 33,96787 u [4,365 %]
35S: 34,96903 u [<< 1 %]
36S: 35,96708 u [0,016 %]
32S: 9,45173 %
33S: 0,07595 %
34S: 0,43449 %
35S: Spuren
36S: 0,00159 %
Radium
226Ra: 226,02541 u [100 %]
226Ra: 70,17648 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 322,081409353 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 3,105 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,003 mol.
Monoisotopische Masse: 321,977137854 Da - bezogen auf 16O432S226Ra.
Synthese, Gewinnung
Zur Darstellung kann Radiumsulfat aus einer Lösung einer anderen Radium-Verbindungen durch Zugabe von verdünnter Schwefelsäure oder eines wasserlöslichen Alkalisulfats als fester Niederschlag gefällt werden - wie zum Beispiel:
RaBr2 + H2SO4 → RaSO4↓ + 2 HBr,
RaBr2 + Na2SO4 → RaSO4↓ + 2 NaBr.
Externe Informationsquellen
Literatur und Quellen
[1] - Artem V. Matyskin, Rikard Ylmen, Petra Lagerkvist, Henrik Ramebäck, Christian Ekberg:
Crystal structure of radium sulfate: An X-ray powder diffraction and density functional theory study.
In: Journal of Solid State Chemistry, (2017), DOI 10.1016/j.jssc.2017.05.024.
Letzte Änderung am 27.02.2024.
Permalink: https://www.internetchemie.info/substanz/Radiumsulfat.php
© 1996 - 2024 Internetchemie ChemLin