|
Bei der Oxidation von Propylen (Propen, CH3CH=CH2) zu Propylenoxid (Propenepoxid) wird formal ein Sauerstoffatom in die Doppelbindung eingeschoben. Es entsteht ein Ring aus zwei Kohlenstoffatomen und einem Sauerstoffatom. Sauerstoff als Oxidationsmittel kam bisher nicht in Betracht, da sich das Sauerstoffmolekül (O2) nur unter Zuführung einer extrem hohen Energiemenge in Sauerstoffatome spalten lässt. Außerdem reagiert Propylen mit atomarem Sauerstoff bevorzugt zu Acrolein und nicht zum gewünschten Propylenoxid. Ein geeigneter Katalysator wird händeringend gesucht und mittlerweile als Heiliger Gral der Katalyseforschung angesehen. Es gibt bereits eine Reihe von Katalysatorentwicklungen, die jedoch noch nicht wirklich überzeugen konnten.
|
 |
|
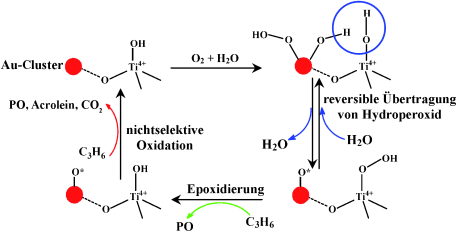
Weniger als 2.0 nm große
Goldcluster - aber keine Goldnanopartikel - auf alkalisiertem
Titansilicalit-1 können aus O2 und H2O
Hydroperoxid (-OOH) erzeugen. Dieses wird auf benachbarte
Ti-Zentren übertragen, wobei Ti-OOH-Gruppen entstehen (siehe
Schema), die Propen in Propenepoxid (PO) umwandeln können.
[Bildquelle: siehe (1)] |
Aufbauend auf früheren Arbeiten haben Haruta und sein Team nun einen weiteren Fortschritt erzielen können. Ihr neuer Katalysator besteht aus weniger als 2 nm großen Goldclustern auf einem speziellen titanhaltigen Silikat als Trägermaterial. Es ist wichtig, dass das Gold nicht in Form von Nanopartikeln vorliegt, sondern als so genannte Cluster, betont Haruta. Auch wenn in der Literatur beide Begriffe oft synonym verwendet werden, gibt es wichtige Unterschiede. Goldcluster sind eindeutig definierte, strukturell einheitliche nanoskopische Gebilde, während unter Goldnanopartikeln Teilchen im Nanometerbereich verstanden werden, die weder in Größe noch in ihrer Struktur einheitlich sind. Unsere Goldcluster sind in der Lage, aus Sauerstoff und Wasser Hydroperoxid zu erzeugen, das auf benachbarte Titanzentren übertragen wird, erläutert Haruta. Die so entstehenden Titanhydroperoxid-Spezies (-Ti-OOH) sind die eigentlichen Reaktionspartner des Propylens, das zu Propylenoxid umgewandelt wird. Noch sind die erzielten Ausbeuten und Selektivitäten für einen industriellen Prozess nicht ausreichend, so Haruta, unser Katalysator ist aber ein weiterer wichtiger Meilenstein auf dem Weg zu einer umweltfreundlichen Propylenoxid-Synthese.
|