Kupfer(II)-sulfat ist eine anorganisch-chemische Verbindung aus der Gruppe der Sulfate; es handelt sich um das Kupfer(II)-Salz der Schwefelsäure.
Das Kupfersulfat mit Cu in der einwertigen Form (Cu(I)) ist das Kupfer(I)-sulfat.
Bezeichnungen und Identifikatoren
Kupfersulfat
CuO4S
CuSO4
159,602 (g/mol)
7758-98-7
231-847-6
ARUVKPQLZAKDPS-UHFFFAOYSA-L
Systematischer Name
Kupfer(II)-sulfat
Weitere Bezeichnungen, Synonyme
Kupfersulfat wasserfrei
INCI-Bezeichnung
COPPER SULFATE
Englische Bezeichnung
Copper sulfate
Copper(II) sulfate; Cupric sulfate anhydrous; Copper sulphate
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Kupfersulfat:
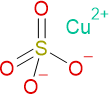
CuO4S oder CuSO4
Mr = 159,602 g/mol
Kupfer(II)-sulfat
SMILES: [O-]S(=O)(=O)[O-].[Cu+2]
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Kupfersulfat. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Wasserfreies Kupfersulfat liegt in reiner Form als grau-weißer, geruchloser, hygroskopischer, kristalliner Feststoff vor, der sich durch Aufnahme von Feuchtigkeit blau verfärbt. Die Substanz bildet Hydrate der allgemeinen Formel CuSO4 × n H2O, wobei n zwischen 1 und 7 liegen kann. Das am häufigsten auftretende und auch kommerziell vermarktete Salz ist das Kupfersulfat-Pentahydrat.
590 °C
3,60 g cm-3 bei 20 °C
-769,98 kJ/mol bei 25 °C
109,2 J/(K mol) bei 25 °C
-662,2 kJ/mol
98,87 J/(mol K)
ε = 10,3 bei 20 °C
(Dielektrizitätskonstante)
+1330 × 10-6 cm3 mol-1
Das wasserfreie Kupfersulfat kristallisiert im orthorhombischen Kristallsystem oP24, Raumgruppe Pnma mit den Gitterkonstanten a = 839 pm, b = 669 pm und c =483 pm.
Kupfersulfat-Lösung:
Kupfersulfat ist in Wasser gut, aber begrenzt löslich. Das Salz löst sich exotherm in Wasser unter Bildung eines blauen Aquokomplex [Cu(H2O)6]2+ mit oktaedrischer Molekülgeometrie sowie Sulfat-Anionen SO42- auf.
Die nachfolgende Tabelle listet neben der Temperatur die maximale Löslichkeit in Gramm pro Liter Wasser, den jeweiligen Massenanteil des Kupfer(II)-sulfats sowie die Molalität b der CuSO4-Lösung:
| Temperatur | Löslichkeit in g/L | Massenanteil | Molalität b | |
|---|---|---|---|---|
| wasserfrei | Pentahydrat | ω (CuSO4) | [mol/kg] | |
| 0 °C | 141,55 | 221,4 | 0,124 | 0,887 |
| 10 °C | 168,22 | 263,2 | 0,144 | 1,054 |
| 20 °C | 200,48 | 313,6 | 0,167 | 1,256 |
| 25 °C | 219,51 | 343,4 | 0,180 | 1,375 |
| 30 °C | 239,16 | 374,1 | 0,193 | 1,498 |
| 40 °C | 285,35 | 446,4 | 0,222 | 1,788 |
| 50 °C | 340,48 | 532,6 | 0,254 | 2,133 |
| 60 °C | 404,49 | 632,8 | 0,288 | 2,534 |
| 70 °C | 479,29 | 749,8 | 0,324 | 3,003 |
| 80 ° C | 569,86 | 891,5 | 0,363 | 3,570 |
| 90 °C | 675,04 | 1056,0 | 0,403 | 4,230 |
| 100 °C | 769,91 | 1204,4 | 0,435 | 4,824 |
Als konzentrationsabhängige Eigenschaften sind nachfolgend die Stoffmengenkonzentration c (Molarität), die Dichte ρ, der Brechnungsindex n sowie die Leitfähigkeit κ (Millisiemens/cm) von Kupfersulfat-Lösungen in Abhängigkeit vom Massenanteil an CuSO4 dargestellt.
Alle Daten beziehen sich auf eine Temperatur von 20 °C.
| Massen- prozente | c [mol/L] | Dichte ρ [g cm-3] | Brechungsindex nD | κ [mS/cm] |
|---|---|---|---|---|
| 0,5 | 0,031 | 1,0033 | 1,3339 | 2,9 |
| 1 | 0,063 | 1,0085 | 1,3348 | 5,4 |
| 2 | 0,128 | 1,0190 | 1,3367 | 9,3 |
| 3 | 0,194 | 1,0296 | 1,3386 | |
| 4 | 0,261 | 1,0403 | 1,3405 | |
| 5 | 0,330 | 1,0511 | 1,3424 | 19 |
| 6 | 0,400 | 1,0620 | 1,3443 | |
| 7 | 0,472 | 1,0730 | 1,3462 | |
| 8 | 0,545 | 1,0842 | 1,3481 | |
| 9 | 0,620 | 1,0955 | 1,3501 | |
| 10 | 0,696 | 1,1070 | 1,3520 | 32,2 |
| 12 | 0,854 | 1,1304 | 1,3560 | |
| 14 | 1,020 | 1,1545 | 1,3601 | |
| 15 | 42,3 | |||
| 16 | 1,193 | 1,1796 | 1,3644 | |
| 18 | 1,375 | 1,2059 | 1,3689 |
Spektroskopische Daten:
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Kupfersulfat - CuO4S - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Kupfer
63Cu: 62,9296 u [69,15 %]
65Cu: 64,92779 u [30,85 %]
63Cu: 27,53227 %
65Cu: 12,28302 %
Sauerstoff
ΣAr = 63,996 u
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 39,99981 %
17O: 0,01538 %
18O: 0,0822 %
Schwefel
32S: 31,97207 u [94,954 %]
33S: 32,97146 u [0,763 %]
34S: 33,96787 u [4,365 %]
35S: 34,96903 u [<< 1 %]
36S: 35,96708 u [0,016 %]
32S: 19,07385 %
33S: 0,15327 %
34S: 0,87682 %
35S: Spuren
36S: 0,00321 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 159,602 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 6,266 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,006 mol.
Monoisotopische Masse: 158,8813267495 Da - bezogen auf 63Cu16O432S.
Verwendung in Kosmetika
INCI-Bezeichnung: COPPER SULFATE
Kupfersulfat ist in der EU ein zugelassener Inhaltsstoff kosmetischer Mittel in der Funktion als hautkonditionierende Komponente.
Quelle: CosIng (Cosmetic Ingredient Database der EU) Nummer: 33031.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)


Signalwort: Achtung
Gefahrenhinweise (H-Sätze):
- H302
Gesundheitsschädlich bei Verschlucken. - H315
Verursacht Hautreizungen. - H319
Verursacht schwere Augenreizung. - H400
Sehr giftig für Wasserorganismen. - H410
Sehr giftig für Wasserorganismen, mit langfristiger Wirkung.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.028.952 sowie Informationen zu REACh unter ECHA Chem 100.028.952.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Kupfersulfat sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 001760.
Weitere unfangreiche toxikologische Daten und Gefahrstoff-Informationen liefert die Datenbank für gefährliche Stoffe (Hazardous Substances Data Bank) unter der Nummer HSDB 916.
Internationales Sicherheitsdatenblatt (SDS, MSDS) siehe ICSC: 0751 [englisch].
Beförderung gefährlicher Güter (Gefahrgut-Kennzeichnung): UN-Nummer 3288.
Hinweis: Die Kennzeichnungspflicht gemäß CLP-Verordnung gilt unter anderem nicht für bestimmte Stoffe und Gemische für Endverbraucherinnen und Endverbraucher, die in Form von Fertigerzeugnissen vorliegen, wie zum Beispiel Arzneimittel, Tierarzneimittel, Kosmetika, bestimmte Medizinprodukte und medizinische Geräte, Lebensmittel oder Futtermittel sowie bestimmte Lebensmittelzusatzstoffe oder Aromastoffe. Hier sind gegebenenfalls gesonderte rechtliche Vorschriften einzuhalten.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Kupfersulfat als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[0] - Fach- und Forschungsartikel in wissenschaftlichen Zeitschriften via PubMed: Copper_sulfate.
Letzte Änderung am 05.08.2024.
Permalink: https://www.internetchemie.info/substanz/Kupfersulfat.php
© 1996 - 2026 Internetchemie ChemLin