Als Salzsäure bezeichnet man Lösungen unterschiedlicher Konzentration von Chlorwasserstoff (HCl) in Wasser. Das HCl dissoziiert in Wasser vollständig zu Chloridionen und hydratisierten Wasserstoffionen (Hydroniumionen), die wiederum wasserstoffgebundene Komplexe mit anderen Wassermolekülen bilden [1].
Bezeichnungen und Identifikatoren
Salzsäure
HCl
HCl × x H2O
36,458 (g/mol)
113962-65-5
231-595-7
VEXZGXHMUGYJMC-UHFFFAOYSA-N
Weitere Bezeichnungen, Synonyme
Chlorwasserstoffsäure; Hydrochlorische Säure; HCl; HCl(aq)
INCI-Bezeichnung
HYDROCHLORIC ACID
Englische Bezeichnung
Hydrochloric Acid
Muriatic acid; Hydronium chloride; Chlorhydric acid; Spirits of salt
chlorane
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Salzsäure:
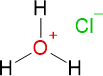
HCl oder HCl × x H2O
Mr = 36,458 g/mol
SMILES: Cl
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Salzsäure. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Die nachfolgenden Angaben beziehen sich auf eine konzentrierte 37 %-ige Salzsäure, die in reinster Form als farblose, häufig jedoch durch Verunreinigungen mehr oder weniger gelblich verfärbte Flüssigkeit vorliegt, die stechend riecht und an der Luft raucht (so genannten rauchende Salzsäure). Weitere Daten: Siehe auch: Salzsäure-Dichtetabelle.
-30 °C
1,19 g cm-3 bei 20 °C
pK1s = -5,9
190 hPa bei 20 °C
Spektroskopische Daten:
splash10-0a4i-0000009000-8651ed5a563be0ad942f
splash10-0a4i-0000009000-6193af2f15253417208c
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Salzsäure - HCl - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Wasserstoff
1H: 1,00783 u [99,99 %]
2H: 2,0141 u [0,01 %]
3H: 3,01605 u [<< 1 %]
1H: 2,76455 %
2H: 0,00028 %
3H: Spuren
Chlor
35Cl: 34,96885 u [75,80 %]
36Cl: 35,96831 u [<< 1 %]
37Cl: 36,9659 u [24,2 %]
35Cl: 73,70426 %
36Cl: Spuren
37Cl: 23,53091 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 36,458 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 27,429 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,027 mol.
Monoisotopische Masse: 35,9766777222 Da - bezogen auf 1H35Cl.
Wirkstoff Salzsäure
Lateinische Bezeichnung: Acidum hydrochloricum.
ATC-Code:A09AB03
B05XA13
In der Medizin wird Salzsäure als saures Digestivum sowie als Additiv von i.v.-Lösungen eingesetzt.
Detail-Informationen zum Wirkstoff in englischer Sprache: Siehe unter DrugBank DB13366 (Wirkstoff-Datenbank), NCI Thesaurus C76716 (Wirkstoff-Beschreibung).
Verwendung in Lebensmitteln
E-Nummer: E507
Salzsäure erfüllt als Lebensmittel-Zusatzstoff (E-Nummer E507) die Funktion eines Säureregulators.
EU: Status und Vorschriften siehe EU Food Additives DB Ref.-Nummer 3205.
Verwendung in Kosmetika
INCI-Bezeichnung: HYDROCHLORIC ACID
Salzsäure ist in der EU ein zugelassener Inhaltsstoff kosmetischer Mittel in der Funktion als Puffersubstanz.
Quelle: CosIng (Cosmetic Ingredient Database der EU) Nummer: 34321.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)


Signalwort: Gefahr
Gefahrenhinweise (H-Sätze):
- H314
Verursacht schwere Verätzungen der Haut und schwere Augenschäden. - H335
Kann die Atemwege reizen.
Die Gefahrstoff-Eigenschaften der Salzsäure sind konzentrationsabhängig. Die konzentrierte Säure (> 25 %) verursacht schwere Hautverätzungen und Augenschäden, während die verdünnte Säure (ab 10 %) haut- und augenreizend wirkt. Die Nebel und Dämpfe sind eine Gefahr für die Atemwege. Beim Erhitzen von Salzsäure wird Chlorwasserstoff freigesetzt!
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.210.665 sowie Informationen zu REACh unter ECHA Chem 100.210.665.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Salzsäure sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 520030.
Weitere unfangreiche toxikologische Daten und Gefahrstoff-Informationen liefert die Datenbank für gefährliche Stoffe (Hazardous Substances Data Bank) unter der Nummer HSDB 545.
Internationales Sicherheitsdatenblatt (SDS, MSDS) siehe ICSC: 0163 [englisch].
Beförderung gefährlicher Güter (Gefahrgut-Kennzeichnung): UN-Nummer 1789.
Hinweis: Die Kennzeichnungspflicht gemäß CLP-Verordnung gilt unter anderem nicht für bestimmte Stoffe und Gemische für Endverbraucherinnen und Endverbraucher, die in Form von Fertigerzeugnissen vorliegen, wie zum Beispiel Arzneimittel, Tierarzneimittel, Kosmetika, bestimmte Medizinprodukte und medizinische Geräte, Lebensmittel oder Futtermittel sowie bestimmte Lebensmittelzusatzstoffe oder Aromastoffe. Hier sind gegebenenfalls gesonderte rechtliche Vorschriften einzuhalten.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Salzsäure als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[0] - Fach- und Forschungsartikel in wissenschaftlichen Zeitschriften via PubMed: Hydrochloric_Acid.
[1] - Noam Agmon:
Structure of Concentrated HCl Solutions.
In: The Journal of Physical Chemistry A, 102, 1, (1998), DOI 10.1021/jp970836x.
Letzte Änderung am 12.04.2025.
Permalink: https://www.internetchemie.info/substanz/Salzsäure.php
© 1996 - 2026 Internetchemie ChemLin