Die Gruppe der Steroide umfasst eine große Zahl überall in der belebten Natur anzutreffender Verbindungen, die sich chemisch gesehen vom Cycopentanoperhydrophenanthren (Steran) ableiten.
Struktur und Nomenklatur
Steran oder Gonan
Steran ist die allgemeine Bezeichnung für das tetracyclische Kohlenstoffskelett Hexadecahydro-cyclopenta[a]phenanthren (I) - ohne Berücksichtigung der stereochemischen Gegebenheiten; die davon abgeleiteten Verbindungen werden als Sterane bezeichnet.
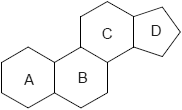 |
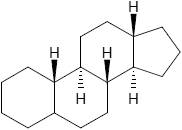 |
| (I) Steran | (II) Gonan |
Betrachtet man das Sterangerüst (I) in der abgebildeten planaren Orientierung, dann können sich Substituenten oberhalb bzw. unterhalb der Molekülebene befinden:
* α-Konfiguration: Substituenten unterhalb der Ebene (alpha-Stellung);
* β-Konfiguration: Substituenten oberhalb der Ebene (beta-Stellung);
* ξ-Konfiguration: Nicht sicher bekannte bzw. unbekannte Stellung des Substituenten (xi).
Durch die 6 chiralen Kohlenstoffatome an den Ring-Verbindungsstellen sind theoretisch 64 Stereoisomere denkbar, von denen tatsächlich jedoch nur sehr wenige auftreten. Für das tetracyclische System aus den mit A, B, C und D bezeichneten Ringen ergeben sich daraus unterschiedliche Möglichkeiten der Ringverknüpfung und damit der Molekülgeometrie:
Die Ringe A/B, B/C und C/D können jeweils cis oder trans miteinander verknüpft sein. Die Ringe B und C der natürlichen Steroide zeigen immer die trans-Konformation.
Gonan ist schließlich ein Stereoisomer des Stenans, bei dem die Ringsysteme B/C und C/D jeweils trans miteinander verbunden sind; die Ringe A/B dürfen eine trans oder eine cis-Konformation aufweisen, woraus für Substituenten an C-5 entweder eine α- (A/B-trans) oder β-Stellung (A/B-cis) resultiert:
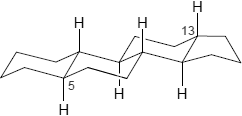 |
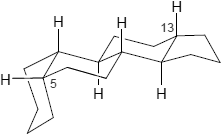 |
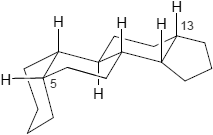 |
| 5α-Gonan | 5β-Gonan | Cardenolid-Typ |
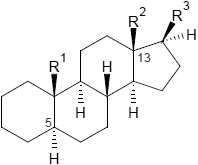 |
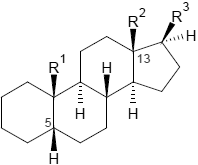 |
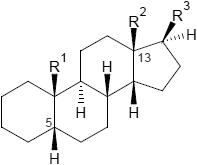 |
| 5α-Steroide | 5β-Steroide | Cardenolide |
| (5α-Reihe: trans-trans-trans) | (5β-Reihe: cis-trans-trans) | (Cardenolid-Reihe: cis-trans-cis) |
Eine cis-trans-cis-Verknüpfung (kein Gonan-System!) der Ringe des Steransystems (Cardenolid-Reihe) weisen die Cardenolide und Bufadienolide auf.
Stereochemischer Bezugspunkt
Zum Beispiel durch Doppelbindungen in den Ringen A und B kann die Molekülgeometrie mehr oder weniger eingeebnet sein. Als stereochemischer Bezugspunkt für die Benennung der cis/trans-Isomeren wurde daher die anguläre Methylgruppe an C-13 gewählt, die sich immer β-ständig - also oberhalb der Ringebene befindet.
Nummerierung des Steroidgerüsts
Die Nummerierung der Kohlenstoff-Atome eines Steroid-Grundgerüsts erfolgt gemäß den Empfehlungen der IUPAC [1] nach folgendem Schema:
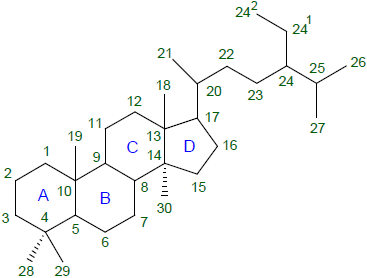
Substituenten unterhalb der Ringebene heißen α-ständig, oberhalb der Ringebene β-ständig; eine unbekannte Konfiguration wird mit ξ im Namen und einer Wellenlinie im Formelbild gekennzeichnet.
Man beachte, dass die Nummerierung 1989 geändert wurde: Vor allem in der älteren Literatur findet man daher die Nummern 28, 29, 30, 31 und 32 an den heute empfohlenen Postitionen 241, 242, 28, 29 und 30.
Ungesättigtes Ringsystem
Doppelbindungen im Stammsystem werden durch Änderung des Stammnamens gekennzeichnet: -en, -adien, -yn. Zur Lokalisation der Doppelbindung sind zwei Methoden geläufig:
* Die von der IUPAC nicht mehr empfohlene (aber häufig anzutreffende) Delta-Nomenklatur verwendet den griechischen Buchstaben Δ - gefolgt von der Position der Doppelbindung als Hochzahl - zur Benennung der Doppelbindung. Befindet sich die Doppelbindung nicht zwischen zwei in der Nummerierung aufeinanderfolgenden Kohlenstoffatomen, dann wird die Zahl des höhernummerierten C-Atoms in Klammern gesetzt. Die Lokanten bei mehreren Doppelbindungen werden durch Kommata getrennt: Ein Δ1,3,5(10)-Estratrien besitzt demnach 3 Doppelbindungen zwischen den Positionen 1/2, 3/4 und 5/10.
* Gemäß den Empfehlungen der IUPAC sollte die Benennung ungesättigter Steroide wie sonst üblich erfolgen. Dabei gilt für die Behandlung der Lokanten das zuvor Gesagte: Δ1,3,5(10)-Estratrien = Estra-1,3,5(10)-trien.
Strukturmodifikationen
Änderungen an der Ringstruktur der Steroide - Ringabbau, Ringwerweiterung, Ringöffnung, Ringumlagerung, Stereoinversion - werden üblicherweise mit entsprechenden Deskriptoren gekennzeichnet - dies bietet vor allem den Vorteil, die Nummerierung des Ringssystems beibehalten und triviale Stammnamen anstelle unhandlicher systematischer Namen weiterverwenden zu können.
Eine Übersicht der Affixe bietet folgende Tabelle. Detailierte Erkläuterungen sind gegebenenfalls unter dem entsprechenden Stichwort zu finden:
| Abeo- | Gerüstumlagerung, gekennzeichnet durch x(y→z)abeo- mit X = unveränderte Postion der umgelagerten Bindung, y = ursprüngliche Position, z = neue Position des umgelagerten Bindungsende. |
| Ent- | Stereochemische Inversion an allen asymmetrischen Zentren. |
| Des- | Fehlender terminaler Ring, gekennzeichnet durch den Großbuchstaben: Des-A-Androstan. |
| Dinor- | Um zwei Methylengruppen verkleinerter Ring bzw. verkleinerte Seitenkette. |
| Dihomo- | Ketten bzw. Ringerweiterung um zwei Methylengruppe. |
| Homo- | Ketten bzw. Ringerweiterung um eine Methylengruppe. |
| Nor- | Um eine Methylengruppe verkleinerter Ring bzw. verkleinerte Seitenkette. |
| Seco- | Bei Ringöffnung unter Angabe der Lokanten: 2,3-Seco-... |
Veraltete Bezeichnungen
| allo | Bezeichnung für A/B-trans-verknüpfte Steroide ohne eigenen Namen. Zur Namensgebung wird dem entsprechenden A/B-cis-verknüften Isomer Allo vorangestellt: Allopregnan = 5α-Pregnan. |
Stammstrukturen
Die Namen foldender Stammverbindungen bzw. Grundstrukturen sind für die Bennung von Steroiden gemäß sind IUPAC-Richtlinien zugelassen:
 |
 |
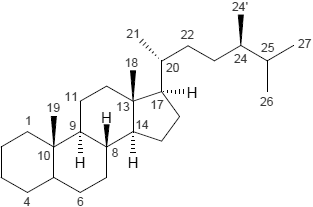 |
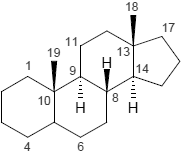
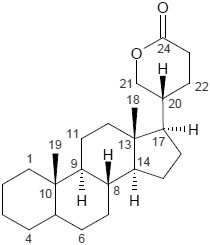
| Androstan | Bufanolid | Campestan |
 |
 |
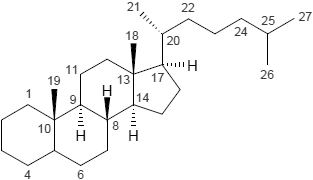 |
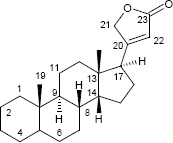
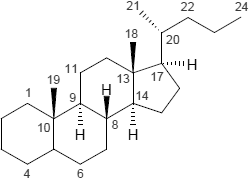
| Cardenolid | Cholan | Cholestan |
 |
 |
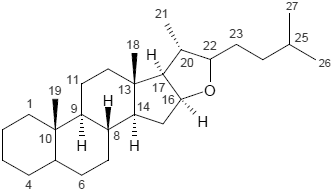 |
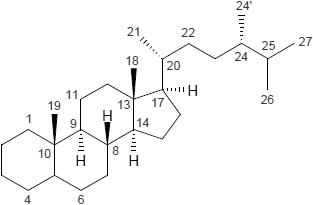
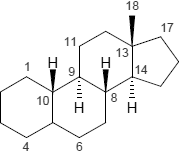
| Ergostan | Estran | Furostan |
 |
 |
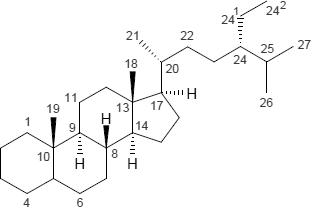 |
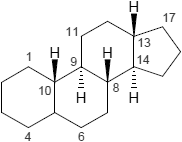
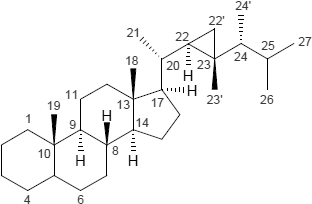
| Gonan | Gorgostan | Poriferastan |
 |
 |
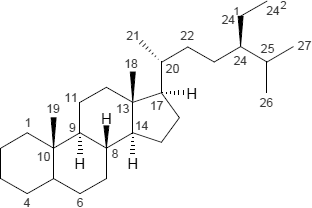 |
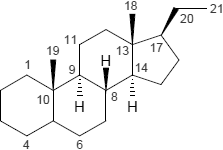
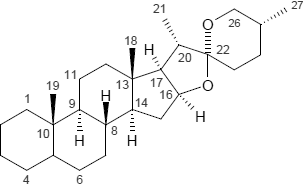
| Pregnan | Spirostan | Stigmastan |
Untergruppen
- Sterole; Oxysterole.
Quellen und weitere Informationen
[1] - The Nomenclature of Steroids. IUPAC-IUB Joint Commission on Biochemical Nomenclature (JCBN).
Kategorie: Stoffgruppen
Aktualisiert am 26. Juni 2023.
Permalink: https://www.internetchemie.info/chemie-lexikon/stoffgruppen/s/steroide.php
© 1996 - 2026 Internetchemie ChemLin