Antimonpentoxid ist eine anorganische Verbindung, die chemisch als das Oxid der Elements Antimon in der Oxidationsstufe V klassifiziert wird.
Bezeichnungen und Identifikatoren
Antimonpentoxid
O5Sb2
Sb2O5
323,515 (g/mol)
1314-60-9
215-237-7
LJCFOYOSGPHIOO-UHFFFAOYSA-N
Systematischer Name
Antimon(V)-oxid
Weitere Bezeichnungen, Synonyme
Diantimonpentoxid; Antimonpentaoxid
Englische Bezeichnung
Antimony pentoxide
Diantimony pentoxide; Antimony(V) oxide; Antimony oxide; Antimony pentaoxide; (Dioxo-λ5-stibanyl)oxy-dioxo-λ5-stibane
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Antimonpentoxid:
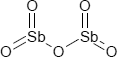
O5Sb2 oder Sb2O5
Mr = 323,515 g/mol
Antimon(V)-oxid
SMILES: O=[Sb](=O)O[Sb](=O)=O
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Antimonpentoxid. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
in reinem Zustand liegt Antimonpentoxid als weißer bis gelblicher, pulvriger Feststoff vor, der praktisch unlöslich in Wasser ist.
380 °C
4,29 g cm-3 bei 21,7 °C
-1008,18 kJ/mol bei 25 °C
0,11769 kJ/(mol K)
Antimonpentoxid hat die gleiche Struktur wie Niob(V)-oxid und kann von der Rutilstruktur abgeleitet werden, wobei Antimon von sechs Sauerstoffatomen in einer verzerrt oktaedrischen Anordnung koordiniert wird. Die SbO6-Oktaeder sind ecken- und kantenverknüpft. Raumgruppe: C2/c Nr. 15 mit a = 1264,6 pm, b = 478,20 pm, c = 542,47 pm sowie β = 103,91 ° [M. Jansen, 1979].
Spektroskopische Daten:
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Antimonpentoxid - O5Sb2 - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Sauerstoff
ΣAr = 79,995 u
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 24,66674 %
17O: 0,00948 %
18O: 0,05069 %
Antimon
ΣAr = 243,52 u
121Sb: 120,90381 u [57,21 %]
123Sb: 122,90421 u [42,79 %]
121Sb: 43,06378 %
123Sb: 32,20939 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 323,515 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 3,091 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,003 mol.
Monoisotopische Masse: 321,782193095 Da - bezogen auf 16O5121Sb2.
Synthese, Gewinnung
Antimonpentoxid kann auf sehr unterschiedliche Arten dargestellt werden - beispielsweise:
Oxidation von Antimontrioxid mit Salpetersäure. Oxidation von elementatem Antimon oder Antimontrioxid an der Luft bei erhöhter Temperatur. Calcinieren von Antimonnitrat.
In heißer wäßriger Lösung entsteht das Oxid als Fällung aus Antimonpentachlorid oder Fluorantimonsäure. Die saure Zersetzung von Hexahydroxyantimonaten führt ebenfalls zum gewünschten Produkt.
Das Oxidhydrat wird durch Hydrolyse von Antimonpentachlorid oder auch durch Ansäuern von Kaliumhexahydroxoantimonat(V) mit verdünnten Säuren hergestellt.
Verwendung
Die Antimon-Verbindung findet Verwendung als Flammschutzmittel in Acrylnitril-Butadien-Styrol-Copolymeren (ABS) und anderen Kunststoffen sowie als Flockungsmittel bei der Herstellung von Titandioxid und wird manchmal bei der Herstellung von Glas, Emaille, Farben und Klebstoffen verwendet. Darüber hinaus dient das Antimonoxid in Austauscherharzen zum Ionenaustausch für eine Reihe von Kationen in saurer Lösung einschließlich Na+ (insbesondere wegen der selektiven Retention) und als Polymerisations- und Oxidationskatalysator. Die Substanz war zudem Bestandteil der Leuchtstoffe von Leuchtstofflampen bestimmter Hersteller. Das Pentoxid kann durch Erhitzen mit Wasserstoff oder Kaliumcyanid zu elementarem Antimon reduziert werden.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)


Signalwort: Achtung
Gefahrenhinweise (H-Sätze):
- H302
Gesundheitsschädlich bei Verschlucken. - H315
Verursacht Hautreizungen. - H319
Verursacht schwere Augenreizung. - H335
Kann die Atemwege reizen. - H411
Giftig für Wasserorganismen, mit langfristiger Wirkung.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.013.853 sowie Informationen zu REACh unter ECHA Chem 100.013.853.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Antimonpentoxid sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 520006.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Antimonpentoxid als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[1] - M. Jansen:
Die Kristallstruktur von Antimon(V)-oxid.
In: Acta Crystallographica Section B, (1979), DOI 10.1107/S056774087900409X.
[2] - L. Yu. Kovalenko, F. A. Yaroshenko, V. A. Burmistrov, T. N. Isaeva, D. M. Galimov:
Thermolysis of Hydrated Antimony Pentoxide.
In: Inorganic Materials, (2019), DOI 10.1134/S0020168519060086.
Letzte Änderung am 12.02.2024.
Permalink: https://www.internetchemie.info/substanz/Antimonpentoxid.php
© 1996 - 2026 Internetchemie ChemLin