
Antimon ist ein chemisches Element mit dem Symbol Sb, welches von der ursprünglichen lateinischen Bezeichnung Stibium abgeleitet wurde. Dem Grundstoff ist die Ordnungszahl 51 zugeordnet; es steht im Periodensystem in der 5. Hauptgruppe (Stickstoff-Gruppe) und stellt in reiner Form ein glänzendes, grauers Halbmetall dar, das vermutlich schon seit der Antike, spätestetens aber seit dem frühen Mittelalter als Antimonium bzw. Stibium (lateinisch) bekannt ist.
Zur Namensherkunft gibt es vielerlei Geschichten; letztlich bleibt sie im Dunkeln. Einige Etymologen glauben, der Begriff stammt vom griechischen Anti-Monachos bzw. dem französischen Antimoine ab; dann hieße Antimon so viel wie Mönchskiller und soll darauf hindeuten, dass frühe Alchemisten Mönche mit Antimon vergiftet haben. Das internationale chemische Zeichen - Sb - wird dem schwedischen Chemiker Jöns Jakob Berzelius zugeschrieben, der die Abkürzung von Stibium abgeleitet hat, der lateinischen Bezeichnung für Antimon.
Übersicht: Allgemeine Daten zum Antimon
Das Antimon-Atom
Das Sb-Atom - und damit das chemische Element Antimon - ist eindeutig durch die 51 positiv geladenen Protonen im Atomkern definiert. Für den elektrischen Ausgleich im ungeladenen Antimon-Atom sorgt die gleiche Anzahl an Elektronen.
Für Unterschiede bei den Atomkernen sorgen die Kernbausteine der Neutronen. Diese Atomsorten werden unter dem Begriff Antimon-Isotope bzw. Sb-Nuklide zusammengefasst (Isotopen-Daten: siehe dort).
Die irdischen Antimon-Vorkommen bestehen aus einem Isotopengemisch; die relative Atommasse wird daher mit 121,760(1) u angegeben.
Elektronenkonfiguration
| Symbol | OZ | Kurzform |
|---|---|---|
| Sb | 51 | [Kr] 4d10 5s2 5p3 |
Langform:
| 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | 5s | 5p | 5d | 5f |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 | 10 | 2 | 3 |
Ionisierungsenergien
Die folgende Tabelle listet die Ionisierungsenergien, also die erforderliche Energie in Elektronenvolt (eV), um ein bestimmtes Elektron von einem Antimon-Atom zu trennen.
| 1. IE: | 8,60839 eV | 2. IE: | 16,63 eV | 3. IE: | 25,3 eV | 4. IE: | 44,2 eV | 5. IE: | 56 eV | 6. IE: | 108 eV |
Elektronenbindungsenergie
Die nachfolgende Tabelle listet die Elektronenbindungsenergien der einzelnen Antimon-Elektronen in den jeweiligen Orbitalen auf. Die Werte sind in Elektronenvolt (eV) angegeben.
| K | LI | LII | LIII |
| 1s | 2s | 2p1/2 | 2p3/2 |
| 30491 | 4698 | 4380 | 4132 |
| MI | MII | MIII | MIV | MV |
| 3s | 3p1/2 | 3p3/2 | 3d3/2 | 3d5/2 |
| 946 | 812,7 | 766,4 | 537,5 | 528,2 |
| NI | NII | NIII | NIV | NV | NVI | NVII |
| 4s | 4p1/2 | 4p3/2 | 4d3/2 | 4d5/2 | 4f5/2 | 4f7/2 |
| 153,2 | 95,6 | 95,6 | 33,3 | 32,1 |
Weitere Daten
145 pm (empirisch, nach Slater)
140 pm (in Einfach-Bindungen, nach Pyykkö et al.)
133 pm (in Zweifach-Bindungen, nach Pyykkö et al.)
127 pm (in Dreifach-Bindungen, nach Pyykkö et al.)
Spektrallinien des Antimons
Die nachfolgende Abbildung zeigt ein Emissionsspektrum des Antimons mit den charakteristischen Spektrallinien im sichtbaren Wellenlängenbereich zwischen 400 und 700 nm:
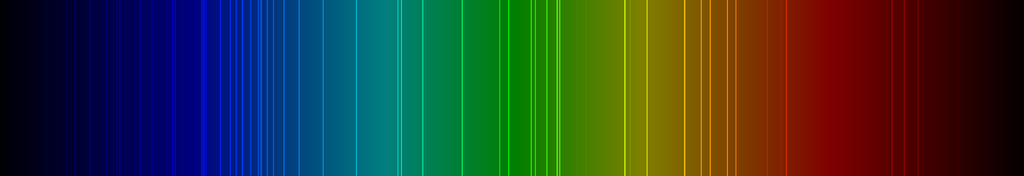
Chemie des Antimons
Als Hauptgruppen-Element in Gruppe 5 (bzw. 15) besitzt Antimon 5 Valenzelektronen; tatsächlich ist aber der Oxidationszustand +III der stabilste, gefolgt von Sb(V). Darüber hinaus sind Antimon-Verbindungen mit den Oxidationszahlen -3 (Antimonide wie beispielsweise das Kaliumantimonid, K3Sb), -2, -1, +1, +2 und +4 bekannt.
Chemische Daten
1,82 nach Allred-Rochow
1,984 nach Allen
2,0 nach Mulliken
2,19 nach Sanderson
5,0203 eV nach Gosh-Gupta
4,85 eV nach Pearson
Standardpotentiale
Normalpotential des Antimons:
| E0 (V) | Nox | Name Ox. | Ox. | e- | ⇔ | Red. | Name Red. | Nox |
| 0,2 | + III | Antimonyl-Kation | SbO+ + 2 H+ | + 3 e- | ⇔ | Sb (s) + H2O | Antimon | 0 |
Material- und physikalische Eigenschaften des Antimons
Die nachfolgende Übersicht führt einige physikalische Daten sowie Materialeigenschaften des reinen Antimons auf.
0,207 J g-1 K-1 (spezifisch)
6,53 g cm-3 (flüssig, am Schmelzpunkt)
nach Brinell: 0,294 GPa
262,3 kJ mol-1 (gasförmig)
180,3 J mol-1 K-1 (gasförmig)
Elementares Antimon ist ein sprödes, silberweiß glänzendes Halbmetall. Beim langsamen Abkühlen kristallisiert geschmolzenes Antimon in einer trigonalen Zelle, isomorph mit dem grauen Allotrop von Arsen. Eine seltene explosive Form von Antimon kann durch Elektrolyse von Antimontrichlorid hergestellt werden. Wenn es mit einem scharfen Werkzeug zerkratzt wird, tritt eine exotherme Reaktion ein und es entstehen weiße Dämpfe als metallische Antimon-Form. Wenn dieses in einem Mörser gerieben wird, kommt es zu einer starken Detonation. Bei schneller Abkühlung des Antimondampfes bildet sich die schwarze Modifikation; Es hat die gleiche Kristallstruktur wie roter Phosphor und schwarzes Arsen, oxidiert an der Luft und kann sich spontan entzünden. Bei 100 °C wandelt es sich allmählich wieder in die stabile Form um. Das gelbe Allotrop von Antimon ist die instabilste Form; sie konnte bisher nur durch Oxidation von Stiban (SbH3) bei - 90 °C erzeugt werden. Oberhalb dieser Temperatur und im Umgebungslicht wandelt sich dieses metastabile Allotrop in die stabilere schwarze Form um.
Literatur und Quellen
[1] - M. L. Dufrenoy, J. Dufrenoy:
The significance of antimony in the history of chemistry.
In: Journal of Chemical Education, 1950, DOI 10.1021/ed027p595.
Externe Informationsangebote
Praktikumsskripten, praktische Anleitungen
Potentiometrische Säure/Base-Titrationen: Antimonsalze
Theorie, Versuchsbeschreibung. Universität Bielefeld
Gruppenelemente - Informationen
Elemente der V. Hauptgruppe (Pnicogene, Pentele)
Vorlesungsskript: Anorganische Strukturchemie. Universität Freiburg
Pentele: Gruppe 15
Vorlesungsunterlagen: Chemie der Elemente. Universität Marburg - Format: PDF
Stickstoffgruppe
Vorlesungsskript zur Chemie der Sauerstoff- und der Stickstoffgruppe. FH Münster - Format: PDF
Einzelne Verbindungen
Antimon und Antimonverbindungen
Chemikalien-Datenbank: Physikalische und chemische Eigenschaften, Sicherheitsdatenblätter, kommerziell verfügbaren Stoffen und Verbindungen; verschiedene Suchkriterien einschließlich Struktursuche
Synthese, Herstellung, Produktion
Rohstoffwirtschaftlicher Steckbrief für Antimon
Übersichten mit Grafiken und Statistiken. BGR
Analyse und Bestimmung
H2S-Gruppe
Der virtuelle Trennungsgang: Schwefelwasserstoffgruppe. Universität Freiburg
Simultane Bestimmung von Arsen-, Selen-, Antimon- und Tellur-Spezies
... mit einer neu entwickelten HPLC/ICP-MS-Kopplung sowie vergleichende Untersuchungen mittels CE/ICP-MS. Dissertation, 2000. Universität Hamburg
Mineralogie
Antimonhaltige Minerale
Informationen zum Antimon und Antimonmineralien. Mineralienatlas
Umweltchemie
Antimon - Ein globaler Schadstoff
Globale Verschmutzung der Erdatmosphäre mit Antimon steigt. Artikel, 2005
Antimon- und Bleibelastung bei Schiessanlagen
Fallbeispiel Eschenbach. ETH Zürich
Toxikologie, Medizin, Physiologie
Toxikologie des Antimons
Gifte.de
Umweltgift Antimon
Eine Zusammenstellung - Format: PDF
Kategorie: Chemische Elemente
Letzte Änderung am 26.08.2021.
Permalink: https://www.internetchemie.info/chemische-elemente/antimon.php.
© 1996 - 2026 Internetchemie ChemLin