Antimonacetat - genauer das Antimon(III)-acetat oder Antimontriacetat - ist eine chemische Verbindung, die als Antimonsalz der Essigsäure beschrieben wird. Die salzartige Antimon-Verbindung besteht aus dreiwertigen Sb(III)-Kationen mit jeweils drei Acetat-Anionen als Gegenionen.
Bezeichnungen und Identifikatoren
Antimonacetat
C6H9O6Sb
298,892 (g/mol)
6923-52-0
230-043-2
JVLRYPRBKSMEBF-UHFFFAOYSA-K
Systematischer Name
Antimon(III)-triacetat
Weitere Bezeichnungen, Synonyme
Antimon(III)-acetat; Antimontriacetat; Antimonazetat
Englische Bezeichnung
Antimony(III) acetate
Antimony(3+) triacetate; Diacetyloxystibanyl acetate
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Antimonacetat:
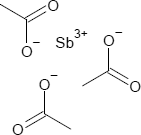
C6H9O6Sb
Mr = 298,892 g/mol
Antimon(III)-triacetat
SMILES: CC(=O)[O-].CC(=O)[O-].CC(=O)[O-].[Sb+3]
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Antimonacetat. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
In reinem Zustand und unter Standardbedingungen liegt Antimon(III)-acetat in Form eines weißen Pulvers vor, das mäßig wasserlöslich ist. Beim Erhitzen zersetzt es sich zu Antimontrioxid.
+ Löslich in Essigsäureanhydrid; mäßig löslich in Wasser unter langsamer Zersetzung.
- Unlöslich in Benzol, Tetrachlorkohlenstoff.
128,5 °C
1,22 g cm-1 bei 25 °C
Monokline Kristalle, der Raumgruppe P21 Nr. 4 mit a = 746,3(5) pm, b = 934,6(5) pm, c = 774,0(5) pm sowie β = 116,20(5)°, Z = 2 [1]. Im Festkörper besteht Antimonacetat aus diskreten Sb(OAc)3-Monomeren mit einzähnigen Acetat-Liganden. Die Monomere sind durch schwache intermolekulare C=O···Sb-Wechselwirkungen zu Ketten verbunden.
Spektroskopische Daten:
Berechnetes NMR-Spektrum (Predict Spectra via NMRDB)
1H NMR Spektrum, 13C NMR Spektrum.
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Antimonacetat - C6H9O6Sb - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Kohlenstoff
ΣAr = 72,066 u
12C: 12 u [98,94 %]
13C: 13,00335 u [1,06 %]
14C: 14,00324 u [<< 1 %]
12C: 23,85547 %
13C: 0,25558 %
14C: Spuren
Wasserstoff
ΣAr = 9,072 u
1H: 1,00783 u [99,99 %]
2H: 2,0141 u [0,01 %]
3H: 3,01605 u [<< 1 %]
1H: 3,03491 %
2H: 0,0003 %
3H: Spuren
Sauerstoff
ΣAr = 95,994 u
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 32,03857 %
17O: 0,01232 %
18O: 0,06584 %
Antimon
121Sb: 120,90381 u [57,21 %]
123Sb: 122,90421 u [42,79 %]
121Sb: 23,30571 %
123Sb: 17,43141 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 298,892 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 3,346 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,003 mol.
Monoisotopische Masse: 297,9437230038 Da - bezogen auf 12C61H916O6121Sb.
Synthese, Gewinnung
Antimonacetat kann durch die Reaktion Antimontrioxid mit Essigsäure hergestellt werden:
Sb2O3 + 6 CH3COOH → 2 Sb(CH3COO)3 + 3 H2O.
Alternativ können geeignete andere Antimon-Salze oder Acetanhydrid eingesetzt werden.
Verwendung
Antimonacetat wird in der chemischen Industrie bei der Herstellung von Kunststoffprodukten und Kunststoffadditiven bzw. als Katalysator bei der Herstellung von synthetischen Polyester-Fasern eingesetzt.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)


Signalwort: Achtung
Gefahrenhinweise (H-Sätze):
- H302
Gesundheitsschädlich bei Verschlucken. - H315
Verursacht Hautreizungen. - H319
Verursacht schwere Augenreizung. - H332
Gesundheitsschädlich bei Einatmen. - H411
Giftig für Wasserorganismen, mit langfristiger Wirkung.
LD50 (Ratte, oral): 4480 mg/kg.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.027.312 sowie Informationen zu REACh unter ECHA Chem 100.027.312.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Antimonacetat als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[1] - Michael Hall, D. Bryan Sowerby:
Antimony(III) acetate and thioacetate: spectra and crystal structures.
In: Dalton Transactions, (1980), DOI 10.1039/DT9800001292.
Letzte Änderung am 12.02.2024.
Permalink: https://www.internetchemie.info/substanz/Antimonacetat.php
© 1996 - 2026 Internetchemie ChemLin