Antimonpentafluorid - auch als Antimon(V)-fluorid bekannt - ist eine binäre anorganisch-chemische Verbindung aus den Elementen Antimon (Oxidationsstufe +V) und Fluor.
Bezeichnungen und Identifikatoren
Antimonpentafluorid
F5Sb
SbF5
216,752 (g/mol)
7783-70-2
232-021-8
VBVBHWZYQGJZLR-UHFFFAOYSA-I
Weitere Bezeichnungen, Synonyme
Antimon(V)-fluorid; Pentafluorostiban; Pentafluorostibin
Englische Bezeichnung
Antimony pentafluoride
Antimony(V) fluoride; Pentafluoridoantimony; Pentafluorostibane; Pentafluorostibine; Pentafluoro-λ5-stibane
Chemische Formeln
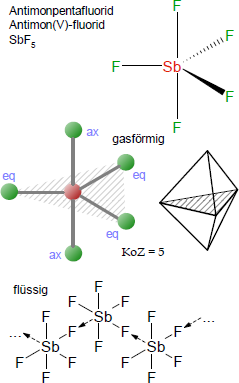
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Antimonpentafluorid:
-fluorid.png)
F5Sb oder SbF5
Mr = 216,752 g/mol
SMILES: F[Sb](F)(F)(F)F
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Antimonpentafluorid. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Antimonpentafluorid liegt in reiner Form unter Standardbedingungen als farblose, stechend riechende, ölige (mäßig viskose), stark hygroskopische Flüssigkeit vor, die heftig mit Wasser sowie verschiedenen anderen Lösungsmitteln reagiert. Zersetzt langsam Glas, Kupfer, Blei und wirkt gegenüber Metallen, insbesondere in Gegenwart von Luftfeuchtigkeit, korrosiv; Ausnahme: Stahl.
8,3 °C
149,5 °C
2,99 g cm-3 bei 20 °C
1,33 kPa bei 25 °C
0,768 cP bei 25 °C
0,20 N/m bei 20 °C
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Antimonpentafluorid - F5Sb - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Fluor
ΣAr = 94,992015815 u
19F: 18,9984 u [100 %]
19F: 43,82521 %
Antimon
121Sb: 120,90381 u [57,21 %]
123Sb: 122,90421 u [42,79 %]
121Sb: 32,1376 %
123Sb: 24,03719 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 216,752015815 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 4,614 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,005 mol.
Monoisotopische Masse: 215,895825815 Da - bezogen auf 19F5121Sb.
Synthese, Gewinnung
Antimonpentafluorid kann unter anderem durch Fluorierung von Antimontrifluorid oder auch durch Umsetzung von Antimonpentachlorid mit Fluorwasserstoff (HF) im Überschuss hergestellt werden:
SbCl5 + 5 HF → SbF5 + 5 HCl.
Bei der letzteren Methode läßt sich das fünfte Chlor-Atom nur mühsam entfernen, was zu Verunreinigungen des Produkts mit Sb(III) führen kann. Die Reinigung erfolgt durch fraktionierende Destillation.
Verwendung
Die Antimon-Verbindung dient aus Ausgangschemikalie für die Synthese anderen Substanzen sowie als Katalysator und ist eine starke Lewis-Säure, ein gutes Oxidations- und Fluorierungsmittel. Die Chemikalie ersetzt leicht alle Chlor-Substituenten in einer organischen Verbindung durch Fluor und fluoriert Doppelbindungen und aromatische Ringe.
Das Chemikalie ist Bestandteil der Supersäure Fluorantimonsäure (HSbF6: pKS = −17), welche aus Antimonpentafluorid und wasserfreiem Fluorwasserstoff im Verhältnis 1:2 besteht.
Gefahren-Hinweise nach GHS
(Allgemeine Hinweise ohne Gewähr auf Richtigkeit und Vollständigkeit! Die Angaben ersetzen weder das Sicherheitsdatenblatt Chemikalien noch eine Gefährdungsbeurteilung, sondern geben eine allgemeine Übersicht hinsichtlich der Gefährdung durch den Gefahrstoff.)




Signalwort: Gefahr
Gefahrenhinweise (H-Sätze):
- H301
Giftig bei Verschlucken. - H311
Giftig bei Hautkontakt. - H314
Verursacht schwere Verätzungen der Haut und schwere Augenschäden. - H332
Gesundheitsschädlich bei Einatmen. - H411
Giftig für Wasserorganismen, mit langfristiger Wirkung.
Zur Kennzeichnung in der EU siehe ECHA Substance Infocard 100.029.110 sowie Informationen zu REACh unter ECHA Chem 100.029.110.
Zur Toxikologie und zum Arbeitsschutz beim Umgang mit Antimonpentafluorid sowie Maßnahmen im Gefahrenfall siehe: Gefahrstoffinformationssystem GESTIS, ZVG-Nr. 500003.
Beförderung gefährlicher Güter (Gefahrgut-Kennzeichnung): UN-Nummer 1732.
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Antimonpentafluorid als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Literatur und Quellen
[1] - Otto Ruff, Wilhelm Plato:
Über die Darstellung und die physikalische Beschaffenheit einiger neuer Fluorverbindungen.
In: Berichte der deutschen chemischen Gesellschaft, (1904), DOI 10.1002/cber.190403701109.
[2] - A. J. Edwards, P. Taylor:
Crystal structure of antimony pentafluoride.
In: Journal of the Chemical Society D: Chemical Communications, (1971), DOI 10.1039/C29710001376.
Letzte Änderung am 12.02.2024.
Permalink: https://www.internetchemie.info/substanz/Antimonpentafluorid.php
© 1996 - 2026 Internetchemie ChemLin