Hexachlorantimonsäure ist eine anorganische Verbindung, die chemisch als das Komplexsalz aus Antimontrichlorid und Chlorwasserstoff charakterisiert wird. Die Salze dieser Säure heissen Hydrogenhexachloroantimonate.
Bezeichnungen und Identifikatoren
Hexachlorantimonsäure
Cl6HSb
H[SbCl6]
335,468 (g/mol)
16941-91-6
NRIYNFREKBKLPQ-UHFFFAOYSA-I
Weitere Bezeichnungen, Synonyme
Hexachlorantimon(V)säure; Wasserstoffhexachlorantimonat
Englische Bezeichnung
Chloroantimonic acid
Hydrogen hexachloroantimonate(1-)
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Hexachlorantimonsäure:
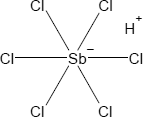
Cl6HSb oder H[SbCl6]
Mr = 335,468 g/mol
SMILES: [H+].Cl[Sb-](Cl)(Cl)(Cl)(Cl)Cl
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Hexachlorantimonsäure. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Die Hexachlorantimonsäure läßt sich nur in Form kristalliner Hydrate wie H[SbCl6] × 4,5 H2O isolieren, das hellgrüne, sehr hygroskopische Kristalle bildet, bei etwa 44 °C schmilzt und in starker Verdünnung wieder hydrolysiert. Das Monohydrat kann durch Trocknen des kristallinen Hydrats über Schwefelsäure gewonnen werden. Beim Versuch, die wasserfreie Substanz zu erhalten, tritt ab etwa 70 °C die Zersetzung zu SbCl5, HCl und Wasser ein. Mit konzentrierten Alkalilaugen lassen sich die Hexahydroxyantimonatsalze und mit Alkalimetallchloriden die jeweiligen Hexachlorantimonate darstellen.
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Hexachlorantimonsäure - Cl6HSb - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Chlor
ΣAr = 212,7 u
35Cl: 34,96885 u [75,80 %]
36Cl: 35,96831 u [<< 1 %]
37Cl: 36,9659 u [24,2 %]
35Cl: 48,0602 %
36Cl: Spuren
37Cl: 15,34376 %
Wasserstoff
1H: 1,00783 u [99,99 %]
2H: 2,0141 u [0,01 %]
3H: 3,01605 u [<< 1 %]
1H: 0,30045 %
2H: 3,0E-5 %
3H: Spuren
Antimon
121Sb: 120,90381 u [57,21 %]
123Sb: 122,90421 u [42,79 %]
121Sb: 20,76469 %
123Sb: 15,53087 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 335,468 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 2,981 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,003 mol.
Monoisotopische Masse: 331,7247511722 Da - bezogen auf 35Cl61H121Sb.
Synthese, Gewinnung
Die Hexachlorantimonsäure läßt sich durch Auflösen von metallischem Antimon bei 30 bis 40 °C in Königswasser (a) sowie von Antimontrioxid (b) oder Antimonpentachlorid (c) in konzentrierter Salzsäure darstellen:
(a) 3 Sb + 18 HCl + 5 HNO3 → 3 H[SbCl6] + 5 NO↑ + 10 H2O,
(b) Sb2O5 + 12 HCl → 2 H[SbCl6] + 5 H2O,
(c) SbCl5 + HCl → H[SbCl6].
Externe Informationsquellen
Hersteller und Bezugsquellen
In der nachfolgenden Tabelle sind Produzenten und Lieferanten von Hexachlorantimonsäure als kommerzielle Chemikalie für Labor, Forschung, Industrie und Produktion mit den entsprechenden Kontaktdaten verzeichnet.
Letzte Änderung am 20.02.2024.
Permalink: https://www.internetchemie.info/substanz/Hexachlorantimonsäure.php
© 1996 - 2026 Internetchemie ChemLin