Dipeptide bilden eine Gruppe chemischer Verbindungen, die aus zwei über eine Peptid-Bindung verbundene Aminosäuren bestehen; formal handelt es sich bei den Dipeptiden um Carbonsäureamide. Sie spielen im Proteinstoffwechsel sowohl beim Auf- wie auch beim Abbau von Peptiden und Proteinen eine zentrale Rolle.
Benennung der Dipeptide
An einem Dipeptid können sowohl zwei gleiche wie auch zwei verschiedene Aminosäuren beteiligt sein. Die 23 proteinogenen Aminosäuren können somit 232 = 529 verschiedene Dipeptide bilden.
Sind die beiden Aminosäuren identisch, dann wird der Name des Aminosäure-Rests dem Namen vorangestellt: Glycylglycin, Alanylalanin.
Bei zwei verschiedenen Aminosäuren wird zunächst die C-Terminale Aminosäure bestimmt - sie liefert den Stammnamen. Der N-terminale Acyl-Rest der zweiten Aminosäure wird dem Namen vorangestellt. Die Stereochemie einmal unberücksicht können also jeweils 2 verschiedene Aminosäuren zwei verschiedene Dipeptide bilden:
Beispiel:
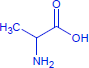 | 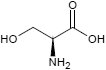 |
| Alanin | Serin |
Die Aminosäuren Alanin (blau) und Serin (schwarz) können auf zwei unterschiedliche Arten zu einem Dipeptid zusammenfinden:
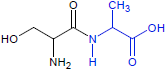 | 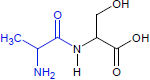 |
| Serylalanin | Alanylserin |
| Alanin: C-terminal | Alanin: N-terminal |
| Serin: N-terminal | Serin: C-terminal |
Statt der ausgeschriebenen Namen werden häufig auch nur die Abkürzungen der beteiligten Aminosäuren verwendet.
Cyclische Dipeptide
Bilden zwei Aminosäuren miteinander ein cyclisches System, dann spricht man von cyclischen Dipeptiden. Die terminalen Funktionen der beteiligten Aminosäuren gehen unter Bildung von cis-Peptidbindungen und eines Lactam-Rings verloren. Die einfachsten Vertreter dieser Stoffgruppe sind die Diketopiperazine, cyclische Dipeptide aus Glycin und L-Alanin bzw. aus zwei Einheiten L-Prolin.
Kategorie: Stoffgruppen
Aktualisiert am 31. März 2022.
Permalink: https://www.internetchemie.info/chemie-lexikon/stoffgruppen/d/dipeptide.php
© 1996 - 2026 Internetchemie ChemLin