Radiumnitrat ist eine radioaktive, sehr giftige, anorganische Verbindung, die chemisch als das Radium-Salz der Salpetersäure beschrieben wird.
Bezeichnungen und Identifikatoren
Radiumnitrat
N2O6Ra
Ra(NO3)2
350,033 (g/mol)
10213-12-4
AMLSLPXXUHKKSF-UHFFFAOYSA-N
Weitere Bezeichnungen, Synonyme
Radiumdinitrat; Radium(II)-nitrat
Englische Bezeichnung
Radium nitrate
Radium dinitrate
Chemische Formeln
Brutto- bzw. Summenformel und Strukturformel der chemischen Verbindung Radiumnitrat:
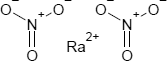
N2O6Ra oder Ra(NO3)2
Mr = 350,0334 g/mol
SMILES: [Ra+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O
Daten und Eigenschaften
Übersicht über die (bekannten) chemischen und physikalischen Eigenschaften: Radiumnitrat. Es gelten - soweit nicht anders angegeben - Raumumgebungsbedingungen (Normaldruck, 0 % Luftfeuchtigkeit, 20 °C).
Die Radium-Verbindung hat in reinem Zustand das Aussehen einer weißen, kristallinen Substanz, die im Dunkeln leuchtet und wasserlöslich ist.
Die Radiumnitrat-Löslichkeit nimmt von etwa 1 × 10-3 auf ca. 2 × 10-5 M ab, wenn die Salpetersäure-Konzentration von 13,5 auf 22 M erhöht wird. Die Löslichkeit von Radiumnitrat ist damit etwa 3 bis 6 mal höher als die Löslichkeit von Bariumnitrat [vgl. P. S. Butkalyuk et al., 2019].
+ Leicht löslich in Wasser (139 g/L bei 20 °C).
- Praktisch unlöslich in 80 %iger Salpetersäure (siehe auch oben).
Prozentuale und isotopische Zusammensetzung:
Massenbezogene elementare Zusammensetzung und Isotopen-Anteile der Verbindung Radiumnitrat - N2O6Ra - berechnet auf Grundlage der Molekülmasse.
.Element E
der Atome Ex
und der Isotope *
der Isotope
Ex an Formelmasse
Stickstoff
ΣAr = 28,014 u
14N: 14,00307 u [99,6205 %]
15N: 15,00011 u [0,3795 %]
14N: 7,97286 %
15N: 0,03037 %
Sauerstoff
ΣAr = 95,994 u
16O: 15,99491 u [99,757 %]
17O: 16,99913 u [0,03835 %]
18O: 17,99916 u [0,205 %]
16O: 27,3576 %
17O: 0,01052 %
18O: 0,05622 %
Radium
226Ra: 226,02541 u [100 %]
226Ra: 64,57252 %
*) Die dritte Spalte führt die Atommassen bzw. Isotopenmassen der beteligten Elemente sowie - in eckigen Klammern - die natürliche Isotopenzusammensetzung auf.
Weitere berechnete Daten
Die molare Masse ist M = 350,033409353 Gramm pro Mol.
Die Stoffmenge von einem Kilogramm der Substanz ist n = 2,857 mol.
Die Stoffmenge von einem Gramm der Substanz ist n = 0,003 mol.
Monoisotopische Masse: 350,0010439225 Da - bezogen auf 14N216O6226Ra.
Synthese, Gewinnung
Die Darstellung des Radiumnitrats erfolgt durch Neutralisation von Radiumcarbonat und Salpetersäure, wobei als Nebenprodukte Wasser und Kohlendioxid gebildet werden:
RaCO3 + 2 HNO3 → Ra(NO3)2 + H2O + CO2&urarr;.
Externe Informationsquellen
Literatur und Quellen
[1] - P. S. Butkalyuk, I. L. Butkalyuk, R. A. Kuznetsov, A. S. Kupriyanov, R. G. Abdullov:
Solubility of Radium Nitrate in Nitric Acid Solutions.
In: Radiochemistry, (2019), DOI 10.1134/S106636221901003X.
Letzte Änderung am 07.08.2024.
Permalink: https://www.internetchemie.info/substanz/Radiumnitrat.php
© 1996 - 2026 Internetchemie ChemLin