Allgemeines
Der Atomradius eines chemischen Elements ist formal der durchschnittliche Abstand bzw. die typische Distanz vom Kernmittelpunkt bis zur äußeren Grenze der zugehörigen Elektronenwolke. Im Verbund mit anderen Atomen kann der Atomradius auch als die kürzeste Distanz ausgelegt werden, bis zu der sich ein zweites Atom annähern kann.
Tatsächlich müssen die Atomradien aus verschiedenen Gründen als rein vergleichende Größen aufgefasst werden; die Bestimmung des absoluten Atomradius ist nicht möglich:
- Die wellenmechanischen Vorstellungen der Quantentheorie erlauben keine definierten Abgrenzungen eines Atoms.
- Die Atomradien variieren je nach Bindungstyp und elektronischer Umgebung.
- Unterschiede der Atomradien der verschiedenen Isotope des betrachteten Elements werden in den Wertetabellen selten berücksichtigt. Häufig wird der Atomradius des stabilsten Isotops angegeben.
Um vergleichbare Werte zu schaffen, gibt es eine Reihe von Wertetabellen, die die Atomradien unter bestimmten Bedingungen angeben: Ionenradien, kovalente Radien, Metallatomradien, Van-der-Waals-Radien und die Radien isolierter Atome.
Periodizität
Generell unterliegen die Atomradien der chemischen Elemente einer Periodizität, die in dem Anwachsen der Kernladung innerhalb einer Periode des Periodensystems und damit in der stärkeren Anziehungskraft des Kerns auf die Elektronen begründet ist: Innerhalb einer Gruppe des PSE nehmen die Radien von oben nach unten zu, innerhalb einer Periode von links nach rechts ab.
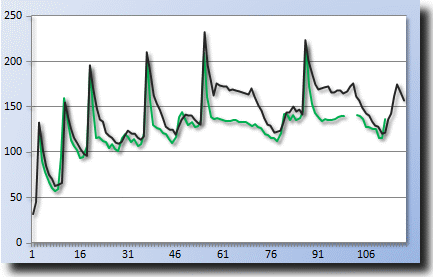 |
| Diagramm: Entwicklung der kovalenten Atomradien (in Picometern, vertikale Achse) bei Einfachbindungen (schwarz) und Doppelbindungen (grün) mit steigender Ordnungszahl (horizontale Achse). |
Tabelle: Atomradien der Elemente
Alle Werte in Picometern: 1 Ångström = 100 pm.
| OZ | Element | Symbol | rber | remp | rkov | rkefb | rkdob | rkdrb | rvdw1 | rvdw2 |
|---|---|---|---|---|---|---|---|---|---|---|
| [1] | [2] | [3] | [3a] | [3b] | [3c] | [4a] | [4b] | |||
| 1 | Wasserstoff | H | 53 | 25 | 31 | 32 | 109 | 120 | ||
| 2 | Helium | He | 31 | 28 | 46 | 140 | 140 | |||
| 3 | Lithium | Li | 167 | 145 | 128 | 133 | 124 | 182 | 182 | |
| 4 | Beryllium | Be | 112 | 105 | 96 | 102 | 90 | 85 | 200 | 153 * |
| 5 | Bor | B | 87 | 85 | 84 | 85 | 78 | 73 | 200 | 192 * |
| 6 | Kohlenstoff | C | 67 | 70 | 76 | 75 | 67 | 60 | 170 | 170 |
| 7 | Stickstoff | N | 56 | 65 | 71 | 71 | 60 | 54 | 155 | 155 |
| 8 | Sauerstoff | O | 48 | 60 | 66 | 63 | 57 | 53 | 152 | 152 |
| 9 | Fluor | F | 42 | 50 | 57 | 64 | 59 | 53 | 147 | 147 |
| 10 | Neon | Ne | 38 | 58 | 67 | 96 | 154 | 154 | ||
| 11 | Natrium | Na | 190 | 180 | 166 | 155 | 160 | 227 | 227 | |
| 12 | Magnesium | Mg | 145 | 150 | 141 | 139 | 132 | 127 | 173 | 173 |
| 13 | Aluminium | Al | 118 | 125 | 121 | 126 | 113 | 111 | 200 | 184 * |
| 14 | Silicium | Si | 111 | 110 | 111 | 116 | 107 | 102 | 210 | 210 |
| 15 | Phosphor | P | 98 | 100 | 107 | 111 | 102 | 94 | 180 | 180 |
| 16 | Schwefel | S | 88 | 100 | 105 | 103 | 94 | 95 | 180 | 180 |
| 17 | Chlor | Cl | 79 | 100 | 102 | 99 | 95 | 93 | 175 | 175 |
| 18 | Argon | Ar | 71 | 71 | 106 | 96 | 107 | 96 | 188 | 188 |
| 19 | Kalium | K | 243 | 220 | 203 | 196 | 193 | 275 | 275 | |
| 20 | Calcium | Ca | 194 | 180 | 176 | 171 | 147 | 133 | 200 | 231 * |
| 21 | Scandium | Sc | 184 | 160 | 170 | 148 | 116 | 114 | 200 | 211* |
| 22 | Titan | Ti | 176 | 140 | 160 | 136 | 117 | 108 | 200 | - |
| 23 | Vanadium | V | 171 | 135 | 153 | 134 | 112 | 106 | 200 | - |
| 24 | Chrom | Cr | 166 | 140 | 139 | 122 | 111 | 104 | 200 | - |
| 25 | Mangan | Mn | 161 | 140 | 150 | 119 | 105 | 103 | 200 | - |
| 26 | Eisen | Fe | 156 | 140 | 142 | 116 | 109 | 102 | 200 | - |
| 27 | Cobalt | Co | 152 | 135 | 138 | 111 | 103 | 96 | 200 | - |
| 28 | Nickel | Ni | 149 | 135 | 124 | 110 | 101 | 101 | 163 | 163 |
| 29 | Kupfer | Cu | 145 | 135 | 132 | 112 | 115 | 120 | 140 | 140 |
| 30 | Zink | Zn | 142 | 135 | 122 | 118 | 120 | 139 | 139 | |
| 31 | Gallium | Ga | 136 | 130 | 122 | 124 | 117 | 121 | 187 | 187 |
| 32 | Germanium | Ge | 125 | 125 | 120 | 121 | 111 | 114 | 200 | 211 * |
| 33 | Arsen | As | 114 | 115 | 119 | 121 | 114 | 106 | 185 | 185 |
| 34 | Selen | Se | 103 | 115 | 120 | 116 | 107 | 107 | 190 | 190 |
| 35 | Brom | Br | 94 | 115 | 120 | 114 | 109 | 110 | 185 | 185 |
| 36 | Krypton | Kr | 88 | 116 | 117 | 121 | 108 | 202 | 202 | |
| 37 | Rubidium | Rb | 265 | 235 | 220 | 210 | 202 | 200 | 303 * | |
| 38 | Strontium | Sr | 219 | 200 | 195 | 185 | 157 | 139 | 200 | 249 * |
| 39 | Yttrium | Y | 212 | 180 | 190 | 163 | 130 | 124 | 200 | - |
| 40 | Zirconium | Zr | 206 | 155 | 175 | 154 | 127 | 121 | 200 | - |
| 41 | Niob | Nb | 198 | 145 | 164 | 147 | 125 | 116 | 200 | - |
| 42 | Molybdän | Mo | 190 | 145 | 154 | 138 | 121 | 113 | 200 | - |
| 43 | Technetium | Tc | 183 | 135 | 147 | 128 | 120 | 110 | 200 | - |
| 44 | Ruthenium | Ru | 178 | 130 | 146 | 125 | 114 | 103 | 200 | - |
| 45 | Rhodium | Rh | 173 | 135 | 142 | 125 | 110 | 106 | 200 | - |
| 46 | Palladium | Pd | 169 | 140 | 139 | 120 | 117 | 112 | 163 | 163 |
| 47 | Silber | Ag | 165 | 160 | 145 | 128 | 139 | 137 | 172 | 172 |
| 48 | Cadmium | Cd | 161 | 155 | 144 | 136 | 144 | 158 | 158 | |
| 49 | Indium | In | 156 | 155 | 142 | 142 | 136 | 146 | 193 | 193 |
| 50 | Zinn | Sn | 145 | 145 | 139 | 140 | 130 | 132 | 217 | 217 |
| 51 | Antimon | Sb | 133 | 145 | 139 | 140 | 133 | 127 | 200 | 206 * |
| 52 | Tellur | Te | 123 | 140 | 138 | 136 | 128 | 121 | 206 | 206 |
| 53 | Iod | I | 115 | 140 | 139 | 133 | 129 | 125 | 198 | 198 |
| 54 | Xenon | Xe | 108 | 140 | 131 | 135 | 122 | 216 | 216 | |
| 55 | Caesium | Cs | 298 | 260 | 244 | 232 | 209 | 200 | 343 * | |
| 56 | Barium | Ba | 253 | 215 | 215 | 196 | 161 | 149 | 200 | 268 * |
| 57 | Lanthan | La | 195 | 207 | 180 | 139 | 139 | 200 | - | |
| 58 | Cer | Ce | 185 | 204 | 163 | 137 | 131 | 200 | - | |
| 59 | Praseodym | Pr | 247 | 185 | 203 | 176 | 138 | 128 | 200 | - |
| 60 | Neodym | Nd | 206 | 185 | 201 | 174 | 137 | 200 | - | |
| 61 | Promethium | Pm | 205 | 185 | 199 | 173 | 135 | 200 | - | |
| 62 | Samarium | Sm | 238 | 185 | 198 | 172 | 134 | 200 | - | |
| 63 | Europium | Eu | 231 | 185 | 198 | 168 | 134 | 200 | - | |
| 64 | Gadolinium | Gd | 233 | 180 | 196 | 169 | 135 | 132 | 172 | - |
| 65 | Terbium | Tb | 225 | 175 | 194 | 168 | 135 | 166 | - | |
| 66 | Dysprosium | Dy | 228 | 175 | 192 | 167 | 133 | 155 | - | |
| 67 | Holmium | Ho | 175 | 192 | 166 | 133 | 196 | - | ||
| 68 | Erbium | Er | 226 | 175 | 189 | 165 | 133 | 202 | - | |
| 69 | Thulium | Tm | 222 | 175 | 190 | 164 | 131 | 200 | - | |
| 70 | Ytterbium | Yb | 222 | 175 | 187 | 170 | 129 | 200 | - | |
| 71 | Lutetium | Lu | 217 | 175 | 187 | 162 | 131 | 131 | 200 | - |
| 72 | Hafnium | Hf | 208 | 155 | 175 | 152 | 128 | 122 | 200 | - |
| 73 | Tantal | Ta | 200 | 145 | 170 | 146 | 126 | 119 | 200 | - |
| 74 | Wolfram | W | 193 | 135 | 162 | 137 | 120 | 115 | 200 | - |
| 75 | Rhenium | Re | 188 | 135 | 151 | 131 | 119 | 110 | 200 | - |
| 76 | Osmium | Os | 185 | 130 | 144 | 129 | 116 | 109 | 200 | - |
| 77 | Iridium | Ir | 180 | 135 | 141 | 122 | 115 | 107 | 200 | - |
| 78 | Platin | Pt | 177 | 135 | 136 | 123 | 112 | 110 | 200 | 175 |
| 79 | Gold | Au | 174 | 135 | 136 | 124 | 121 | 123 | 200 | 166 |
| 80 | Quecksilber | Hg | 171 | 150 | 132 | 133 | 142 | 200 | 155 | |
| 81 | Thallium | Tl | 156 | 190 | 145 | 144 | 142 | 150 | 200 | 196 |
| 82 | Blei | Pb | 154 | 180 | 146 | 144 | 135 | 137 | 200 | 202 |
| 83 | Bismut | Bi | 143 | 160 | 148 | 151 | 141 | 135 | 200 | 207 * |
| 84 | Polonium | Po | 135 | 190 | 140 | 145 | 135 | 129 | 200 | 197 * |
| 85 | Astat | At | 150 | 147 | 138 | 138 | 200 | 202 * | ||
| 86 | Radon | Rn | 120 | 150 | 142 | 145 | 133 | 200 | 220 * | |
| 87 | Francium | Fr | 260 | 223 | 218 | 200 | 348 * | |||
| 88 | Radium | Ra | 215 | 221 | 201 | 173 | 159 | 200 | 283 * | |
| 89 | Actinium | Ac | 195 | 215 | 186 | 153 | 140 | 200 | - | |
| 90 | Thorium | Th | 180 | 206 | 175 | 143 | 136 | 200 | - | |
| 91 | Protactinium | Pa | 180 | 200 | 169 | 138 | 129 | 200 | - | |
| 92 | Uran | U | 175 | 196 | 170 | 134 | 118 | 200 | 186 | |
| 93 | Neptunium | Np | 175 | 190 | 171 | 136 | 116 | 200 | - | |
| 94 | Plutonium | Pu | 175 | 187 | 172 | 135 | 200 | - | ||
| 95 | Americium | Am | 175 | 180 | 166 | 135 | 200 | - | ||
| 96 | Curium | Cm | 169 | 166 | 136 | 200 | - | |||
| 97 | Berkelium | Bk | 168 | 139 | 200 | - | ||||
| 98 | Californium | Cf | 168 | 140 | 200 | - | ||||
| 99 | Einsteinium | Es | 165 | 140 | 200 | - | ||||
| 100 | Fermium | Fm | 167 | 200 | - | |||||
| 101 | Mendelevium | Md | 173 | 139 | 200 | - | ||||
| 102 | Nobelium | No | 176 | 200 | - | |||||
| 103 | Lawrencium | Lr | 161 | 141 | 200 | - | ||||
| 104 | Rutherfordium | Rf | 157 | 140 | 131 | 200 | - | |||
| 105 | Dubnium | Db | 149 | 136 | 126 | 200 | - | |||
| 106 | Seaborgium | Sg | 143 | 128 | 121 | 200 | - | |||
| 107 | Bohrium | Bh | 141 | 128 | 119 | 200 | - | |||
| 108 | Hassium | Hs | 134 | 125 | 118 | 200 | - | |||
| 109 | Meitnerium | Mt | 129 | 125 | 113 | 200 | - | |||
| 110 | Darmstadtium | Ds | 128 | 116 | 112 | 186 | - | |||
| 111 | Roentgenium | Rg | 121 | 116 | 118 | - | ||||
| 112 | Copernicium | Cp | 122 | 137 | 130 | - | ||||
| 113 | Nihonium | Nh | 136 | - | ||||||
| 114 | Flerovium | Fl | 143 | - | ||||||
| 115 | Moscovium | Mc | 162 | - | ||||||
| 116 | Livermorium | Lv | 175 | - | ||||||
| 117 | Tenness | Ts | 165 | - | ||||||
| 118 | Oganesson | Og | 157 | - |
Quellen und weitere Informationen
Berechnete Atomradien: rber
[1.1] - E. Clementi, D. L. Raimondi, W. P. Reinhardt:
Atomic Screening Constants from SCF Functions. II. Atoms with 37 to 86 Electrons.
J. Chem. Phys., (1967), DOI 10.1063/1.1712084.
Empirische Daten: remp
[2.1] - J. C. Slater:
Atomic Radii in Crystals.
Journal of Chemical Physics, (1964), DOI 10.1063/1.1725697.
Kovalente Atomradien: rkov
[3] - Beatriz Cordero et al.:
Covalent radii revisited.
Dalton Transactions, (2008), DOI 10.1039/B801115J.
Kovalenzradien für Atome in Einfachbindungen: rkeib
[3a.1] - Pekka Pyykkö, Michiko Atsumi:
Molecular Single-Bond Covalent Radii for Elements 1 - 118.
Chemistry - A European Journal, (2008), DOI 10.1002/chem.200800987.
Kovalenzradien für Atome in Doppelbindungen: rkdob
[3b.1] - Pekka Pyykkö, Michiko Atsumi:
Molecular Double-Bond Covalent Radii for Elements Li-E112.
Chemistry - A European Journal, (2009), DOI 10.1002/chem.200901472.
Additive Kovalenzradien für Atome in Dreifachbindungen: rkdfb
[3c.1] - S. Riedel, P.Pyykkö, M. Patzschke:
Triple-Bond Covalent Radii.
Chemistry - A European Journal, (2005), DOI 10.1002/chem.200401299.
Van-der-Waals-Radien: rvdw1 und rvdw2
[4a] - A. Bondi:
Van der Waals Volumes and Radii.
The Journal of Physical Chemistry, (1964), DOI10.1021/j100785a001.
[4b] - M. Mantina, A.C. Chamberlin, R. Valero, C.J. Cramer, D.G. Truhlar:
Consistent van der Waals Radii for the Whole Main Group.
The Journal of Physical Chemistry, (2009), DOI 10.1021/jp8111556.
Kategorie: Chemische Elemente
Letzte Änderung am 29. November 2022.
Permalink: https://www.internetchemie.info/chemische-elemente/atomradien.php.
© 1996 - 2026 Internetchemie ChemLin